Статья на конкурс «био/мол/текст»: Эпилепсия — одно из широко распространенных нервных заболеваний, характеризующееся прежде всего возникновением судорог. Ее терапия включает в себя длительный (часто пожизненный) прием противоэпилептических препаратов (ПэП). До 40% страдающих от эпилепсии — женщины детородного возраста. Для матерей-эпилептиков особенно опасным является то, что им приходится принимать ПэП в больших дозах во время беременности. Прием ПэП-медикаментов (например вальпроата) может приводить к нарушениям развития эмбриона — т.н. фетальный вальпроатный синдром, который приводит к структурным дефектам почти всех систем организма, отставанию в развитии и к умственной неполноценности.
Эпилепсия и ее терапия
Рисунок 1. Генри Перш: Исцеление женщины с падучей болезнью в последовательной серии изображений, из «Книги деяний Святого Луи», 15-й век.
сайт epilepsiemuseum.de
Эпилепсия является патологией, известной человечеству еще в древности (падучая болезнь — одно из первых названий этого недуга; лечили ее изгнанием бесов из тела жертвы — говорят, некоторым помогало; рис. 1). Она может затрагивать сенсорные, моторные, вегетативные функции, память, поведение, эмоциональный статус, восприятие, речь, поведение. Само определение болезни вызывало споры на протяжении долгого времени, пока, наконец, в 2005 г. Международная лига борьбы с эпилепсией не утвердила следующие постулаты:
- Эпилепсия является общим названием для целой группы заболеваний, отражающих последствия дисфункции мозга.
- Эпилепсия — это мозговое расстройство, характеризующееся стойкой предрасположенностью к возникновению припадков и их нейробиологическими, когнитивными, психологическими и социальными последствиями.
- Эпилептический припадок — это кратковременное проявление признаков и/или симптомов, относящихся к аномально чрезмерной или синхронной нейрональной активности мозга.
- Для постановки диагноза требуется хотя бы один эпилептический припадок.
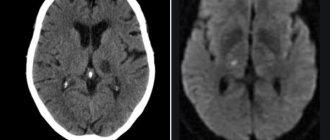
Сегодня около 2% людей во всем мире страдают от эпилепсии, что характеризует ее как одно из самых распространенных неврологических заболеваний. Если не вдаваться в подробности, то возникновение эпилептического припадка вызывается дисбалансом тормозной (основной медиатор — γ-аминомасляная кислота, ГАМК) и возбуждающей (основной медиатор — глутамат) систем головного мозга [8]. Перед припадком действие глутамата намного пересиливает действие ГАМК в какой-либо области мозга, и нейроны этой области начинают генерировать электрические импульсы не разрозненно, как это происходит обычно, а синхронно. Возникает т.н. эпилептический очаг, где клетки разряжаются одновременно. На электроэнцефалограмме (ЭЭГ) можно наблюдать ужасающую картину (рис. 2).
Рисунок 2. Сравнение электроэнцефалограмм здорового пациента и пациента с ювенильными миоклоническими судорогами (одной из форм наследственной эпилепсии, проявляющейся в пубертате).
Children’s hospital of Pittsburgh
Прием лекарств является в настоящее время первой и самой важной частью лечения эпилепсии. Обычно рекомендуется начинать с монотерапии противоэпилептическими препаратами (ПэП), что позволяет подавитьприкадки или хотя бы минимизировать частоту приступов у 50–70% пациентов. Для лечения пациентов, которым монотерапия не помогает, используется политерапия, т.е. сочетание нескольких антиконвульсантов. Среди часто используемых ПэП можно назвать вальпроевую кислоту, вигобатрин, тиагабин, ламотриджин, окскарбамозепин, фельбамат, топирамат, габапентин, леветирацетам, зонисамид, прегабалин. Если же медикаментозное лечение не помогает и в этом случае, то используют крайние меры: хирургическое иссечение эпилептогенного очага, кетогенную диету и глубокую вагусную стимуляцию мозга [16], [19].
Для многих ПэП сначала было показано их антиконвульсаторное (т.е., препятствующее возникновению припадка) действие, а затем уже начали выяснять конкретный механизм, по которому препарат предотвращает развитие припадка. Например, лекарство может влиять на работу потенциал-чувствительных ионных каналов и не давать клетке возможность генерировать потенциал действия; может усиливать влияния ГАМК-ергичекой системы, вызывать ослабление влияния глутаматергической системы через рецепторы медиатора, может влиять непосредственно на высвобождение медиаторов. Для части лекарств характерно сочетание нескольких вышеприведенных механизмов [8], [16].
Однако одновременно с изучением терапевтической активности препаратов начали выявляться серьезные побочные эффекты, характерные для ПэП. Поэтому лечение в каждом случае должно подбираться индивидуально, с учетом особенностей конкретного пациента. Особую группу риска представляют женщины-эпилептики детородного возраста, потому что для них стоит не только вопрос, как забеременеть (ПэП изменяют обмен веществ организма и его гормональный фон), но и как сохранить здоровье будущему ребенку — ведь все ПэП тератогенны, т.е. вызывают у ребенка и физические, и умственные дефекты.
Вальпроевая кислота
Одним из самых широко применяемых и изученных препаратов для лечения эпилепсии является вальпроевая кислота. Она помогает в разных дозах пациентам при практически всех разновидностях судорог, в любом возрасте, и именно ее назначают врачи, когда нужно купировать (заблокировать) припадок у пациента с неизвестной этиологией заболевания.
Рисунок 3. Вальпроевая кислота. Слева — химическая структура вальпроевой кислоты. Справа — Валериана лекарственная, из которой ее получают.
Вальпроевая кислота (встречается в литературе как ВПК или анион соли вальпроат) — производное валерьяновой кислоты, получаемой из эфирного масла травянистого растения валерианы лекарственной (Valeriana officinalis). ВПК была открыта в 1882 году Бартоном (B. Burton), но только в 1963 году было обнаружено ее противосудорожное действие. На сегодня, вальпроевую кислоту используют не только в спектре эпилептических заболеваний, но и при лечении биполярных нарушений, старческой деменции, лейкемии, шизофрении, мигрени, депрессиях. Антиэпилептическое действие препарата обычно связывают с тем, что он повышает тормозную активность ГАМК через увеличение ее синтеза и уменьшение деградации. Также показано нейропротекторное действие вальпроата [1], [8]. Известно, что в зоне судорожного очага нейроны повреждаются, но при введении ВПК до припадка или сразу после него, доля погибших клеток намного снижается, и снабжение клеток питательными веществами (нейротрофика) усиливается. (В частности, такое действие наблюдалось в гиппокампе — части головного мозга, ответственной за формирование памяти и ориентировки в пространстве.)
Однако лечение вальпроатом оказывает и непосредственное негативное воздействие на организм пациента-эпилептика, причем, чем выше доза препарата, тем больше обнаруживается нарушений в организме. Если говорить о самых частых проявлениях, то это увеличение массы тела, метаболические осложнения, уменьшение ночной продолжительности сна, панкреатит, острая печеночная недостаточность, коагулопатии, различные реакции гиперчувствительности, энцефалопатия, эмоциональные расстройства, депрессия, нарушения функционирования эндокринной и репродуктивной систем. Последнее особенно отчетливо проявляется у женщин: синдром поликистоза яичников, нарушения фармакокинетики пероральных контрацептивов, нарушения менструального цикла [2], [19]. Кроме того, ВПК затрудняет процесс имплантации эмбриона на начальных стадиях беременности, понижая экспрессию необходимых для этого белков (ламинина, коллагена-IV и виментина) [6]. И именно вальпроевая кислота является самым опасным препаратом для беременных женщин: она легко проникает через плацентарный барьер [3] и вызывает множество необратимых изменений зародыша.
В 1984 году впервые был описан фетальный вальпроатный синдром [4], при котором характерно возникновение мальформаций (структурных дефектов; рис. 4) сердечно-сосудистой и мочеполовой систем, скелета, черт лица; появляются аномалии глаз и центральной нервной системы (самое типичное для вальпроата — незакрытие нервной трубки), респираторного тракта [7], [18]. Само физическое развитие после рождения замедляется: дети меньше весят и медленнее растут, чем их сверстники. Частота таких явлений при монотерапии ВПК в три раза выше по сравнению с монотерапией любым другим ПэП.
Рисунок 4. Мальформации при фетальном вальпроатном синдроме.
[7]
Встает вопрос: что же может принести больший вред ребенку? Эпилептический припадок матери во время беременности (а это как минимум резкое уменьшение поступления кислорода в мозг плода, как максимум — его гибель) или лекарственная терапия для предотвращения развития этого припадка? Рассматривая статистику, подсчитанную для людей, на этот вопрос ответить практически невозможно. Поэтому проводят исследования на моделях животных, — в частности, на крысах.
Автор этой статьи взяла четыре группы крыс:
- Контрольная группа.
- Группа, получающая вальпроат натрия внутрибрюшинно в течение всего первого триместра беременности.
- Группа, у которой два раза за первый триместр — до и после имплантации зародыша в стенку матки — вызывались эпилептические припадки классическим химическим конвульсантом пентилентетразолом (ПТЗ), ингибитором постсинаптического торможения нейронов центральной нервной системы.
- Группа, которой вводился как вальпроат натрия каждый день первого триметра, так и дважды вводился ПТЗ (но судороги на фоне ВПК не развивались).
Оказалось, что неблагоприятные исходы беременностей присутствовали во всех группах, кроме контрольной (для группы, получавшей ВПК, — 87,8%; для группы, подвергшейся эпилептическим припадкам вследствие введения ПТЗ, — 50%, для группы, получавшей и ВПК, и ПТЗ, — 100%), однако только у крысят, подвергавшихся только действию ВПК in utero, наблюдалось сильное замедление физического развития (критерии: открытие глаз, набор массы и рост вплоть до взрослого состояния) и увеличение тревожности в поведенческих тестах. Также крысятам уже в выросшем состоянии проводилась МРТ-диагностика, опять же выявившая нарушения в основном в группе, получавшей только вальпроат: на рис. 5 крупные белые пятна на верхней линейке рисунков означают расширение желудочков мозга. Уменьшаются объемы и изменяется клеточная структура многих частей головного мозга:
- таламуса (посредник передачи сенсорных и моторных сигналов в кору головного мозга из низлежащих отделов нервной системы);
- бледного шара и стриатума (это базальные ядра, часть экстрапирамидальной системы, участвуют в планировании и осуществлении движений, влияют на мышечный тонус);
- миндалины (часть лимбической стстемы, отвечает не только за формирование положительных эмоций, но и за чувство страха, агрессии, беспокойства);
- гиппокампа (отвечает за пространственную ориентацию и перезапись информации из кратковременной памяти в долговременную, его объем достоверно уменьшался во всех группах по сравнению с контролем).
Рисунок 5. Томографические срезы мозга двухмесячных крыс, получавших ВПК пренатально в первом триместре (A—D), и крыс из контрольной группы (E—H), режим Т2 RARE. Явственно видны расширения желудочков мозга у опытной группы.
исследование автора статьи
Таким образом, мы можем говорить о том, что пренатальное действие вальпроата может влиять на физическое развитие плода и изменять структуру головного мозга на всю последующую жизнь, затрагивая и моторные функции, и процесс формирования эмоций, и память, и поведение в целом, и это воздействие куда более губительно, чем действие самого припадка.
В других исследованиях обнаружено, что крысята, подвергавшиеся in utero действию ВПК (доза 600–800 мг/кг), меньше весили, их развитие замедлялось, они обладали пониженной болевой чувствительностью и, напротив, повышенной чувствительностью к неболевым стимулам, локомоторной гиперактивностью и стереотипией в сочетании с низкой исследовательской мотивацией, пониженным уровнем социального поведения; у них наблюдалось уменьшенное акустическое преимпульсное ингибирование (т.е. снижение моторной реакции на резкий звук). Обычно такие же нарушения выявляют в патологиях аутизма [12], [14].
Сейчас все активнее исследуют влияние вальпроата не только на животных моделях, но и на людях, изучая статистику отклонений и проводя психологические тесты. Корреляцию между внутриутробным влиянием ВПК и развитием заболеваний спектра аутизма можно считать доказаной: IQ у детей дошкольного и школьного возрастов и склонность с общению ниже нормы, внимание и обучаемость нарушены [11], [15], [17].
Лекарственные препараты для лечения COVID-19
Министерство здравоохранения Российской Федерации периодически обновляет методические рекомендации по профилактике, диагностике и лечению коронавируса нового типа. Недавно был расширен список возможных для применения лекарственных средств при лечении заболевания у взрослых. Анализ литературных данных по клиническому опыту ведения пациентов с атипичной пневмонией, связанной с коронавирусами SARS-CoV и MERS-CoV, позволяет выделить несколько этиотропных препаратов, которые рекомендовано использовать в комбинации. К ним относятся хлорохин, гидроксихлорохин, лопинавир + ритонавир, азитромицин (в комбинации с гидроксихлорохином), препараты интерферонов. Среди препаратов, которые находятся на стадии клинических испытаний у пациентов с COVID-19, можно отметить также умифеновир, ремдесивир, фавипиравир [4].
В мировой практике в терапии COVID-19 применяются нижеуказанные противовирусные и противопаразитарные препараты.
Атазанавир
(Atazanavir) — противовирусное средство, являющееся азапептидным ингибитором протеазы ВИЧ. Селективно ингибирует вирус-специфический процессинг вирусных Gag-Pol полипептидов в ВИЧ-инфицированных клетках, предотвращая образование зрелых вирионов и заражение других клеток. Безопасен к применению при беременности [5]. Наряду с другими ингибиторами протеаз ВИЧ применяется в качестве экспериментальной терапии SARS-CoV-2 [6].
Лопинавир/ритонавир
(Lopinavir/ritonavir) — комбинированное противовирусное лекарственное средство. Лопинавир является ингибитором протеазы ВИЧ-1 и ВИЧ-2 и обеспечивает противовирусную активность данной комбинации. Ингибирование ВИЧ-протеаз препятствует синтезу белков вируса и предотвращает расщепление полипептида Gag-Pol, что приводит к образованию незрелого и неспособного к инфицированию вируса. Ритонавир ингибирует опосредованный изоферментом CYP3A4 (цитохром P450 3A4) метаболизм лопинавира в печени, что приводит к повышению концентрации лопинавира в плазме крови, также ритонавир является ингибитором протеазы ВИЧ. Комбинация двух лекарственных средств нивелировала побочные эффекты отдельных средств [7]. Данное комбинированное противовирусное средство применяется для лечения COVID-19, но показало низкую эффективность при тяжелых формах заболевания [8].
Дарунавир/кобицистат
(Darunavir/cobicistat). Дарунавир, так же как и лопинавир, является ингибитором протеазы ВИЧ, а кобицистат повышает эффективность дарунавира путем блокирования изофермента CYP3A. Применяется в качестве экспериментального препарата для лечения COVID-19. Однако исследования показали его неэффективность в профилактике COVID-19 у пациентов с ВИЧ, также ставится под сомнение эффективность данного препарата в отношении SARS-CoV-2 [9].
Ремдесивир
(Remdesivir, код разработки GS-5734) — новое противовирусное средство, разработанное совместно Медицинским исследовательским институтом инфекционных заболеваний Армии США и американской компанией Gilead Sciences для лечения вирусов Эбола и Марбург. Ремдесивир снижает продуцирование вирусной РНК, а в случае с вирусом Эбола обрывает цепи вирусной РНК, способен вызывать инактивирующие вирус мутации. В исследованиях показано, что вещество воздействует и на другие одноцепочные РНК-содержащие вирусы, такие как респираторно-синцитиальный вирус, вирус Джунина, вирус лихорадки Ласса, вирус Нипах, вирус Хендра и коронавирусы (включая вирусы MERS и SARS) [10].
Фавипиравир
(Favipiravir) — противовирусный препарат, селективный ингибитор вирусной РНК-зависимой РНК-полимеразы, также индуцирует летальные мутации РНК-трансверсии, производя нежизнеспособный вирусный фенотип [11]. С 2014 г. одобрен к применению как противогриппозный препарат в Японии. Применяется как экспериментальный препарат для лечения COVID-19. Запрещен к применению у беременных, т. к. в доклинических исследованиях были выявлены тератогенный и эмбриотоксический эффекты [12].
Хлорохин
(Chloroquine) — противомалярийный лекарственный препарат из группы производных 4-аминохинолина. Тормозит синтез нуклеиновых кислот в клетках и обладает умеренным иммуносупрессивным, специфическим и неспецифическим противовоспалительным действием. Применяется для профилактики и лечения малярии, вызывая гибель эпитроцитарных форм большинства видов плазмодиев (кроме
Plasmodium falciparum
), а также эффективен в отношении
Entamoeba histolytica
. В качестве иммуносупрессивного и противовоспалительного препарата эффективен при ревматоидном артрите, системной красной волчанке, аутоиммунном гломерулонефрите, саркоидозе, склеродермии, фотодерматозах [13]. В качестве экспериментального препарата применяется при лечении COVID-19 [14].
Гидроксихлорохин
(Hydroxychloroquine) — противомалярийный препарат, производное 4-аминохинолина. Оказывает также умеренное иммуносупрессивное, специфическое и неспецифическое противовоспалительное действие при аутоиммунных заболеваниях, что расширяет его показания для терапии многих системных заболеваний. Препарат применяется при лечении COVID-19, особенно осложненном наличием сахарного диабета [15]. Наиболее эффективен в комбинации с азитромицином, способствуя ускоренной элиминации вируса из организма, а также в борьбе с присоединяющейся бактериальной флорой в профилактике пневмоний [16]. Гидроксихлорохин входит в перечень жизненно необходимых и важнейших лекарственных препаратов, был одобрен Минздравом России для лечения коронавирусной инфекции [4].
Нитазоксанид
(Nitazoxanide) — противопротозойный и противовирусный препарат, чаще применяемый против вирусов гепатита В и С. Имеются данные, что лекарство обладает противораковым действием (при онкопроцессах в простате, яичниках и кишечнике) [17]. Применяется в качестве экспериментального препарата при COVID-19 [18].
Рибавирин
(Ribavirin) — противовирусный препарат, активный в отношении ряда ДНК- и РНК-содержащих вирусов, является антиметаболитом нуклеозидов и препятствует репликации геномов вирусов. Показана эффективность рибавирина против вирусов гриппа и многих вирусных геморрагических лихорадок, он применяется для лечения тяжелой инфекции, вызванной респираторно-синцитиальным вирусом, вирусного гепатита C и др. Рибавирин активен в форме метаболита, который имеет структуру, сходную с пуриновым нуклеотидом гуанином. Один из побочных эффектов рибавирина — гемолитическая анемия, которая может привести к летальному исходу (данный побочный эффект является дозозависимым). Также рибавирин, как было показано в доклинических исследованиях, обладает тератогенным эффектом, поэтому он запрещен для применения у беременных [19]. Рибавирин используется в качестве экспериментального препарата при COVID-19 [18].
Тоцилизумаб
(Tocilizumab) является иммуносупрессором и применяется главным образом для лечения ревматоидного артрита и системного ювенильного идиопатического артрита. Представляет собой гуманизированное моноклональное антитело против рецептора интерлейкина-6 (IL-6R), связывает растворимые и мембранные рецепторы IL-6, препятствуя провоспалительному действию, блокирует возникновение так называемого «цитокинового шторма», вызывающего шок и гипоксемию. Препарат успешно опробован китайскими специалистами при COVID-19 [20].
Осельтамивир
(Oseltamivir) — осельтамивира фосфат, представляющий собой «пролекарство», которое в организме превращается в осельтамивира карбоксилат, являющийся ингибитором нейраминидазы, используемой вирионами гриппа типов A и B для выхода из клетки. Также осельтамивир применяется в качестве экспериментального препарата для лечения COVID-19 [21].