Болезнь Шарко-Мари-Тута относится к группе разнородных генетических заболеваний, для которых характерно поражение периферической нервной системы с развитием атрофии мышц конечностей. Наряду с этим происходит потеря чувствительности, снижение сухожильных рефлексов и деформация конечностей. Заболевание генетически разнородно, к его возникновению может привести около 40 мутаций, локализованных более чем в 20 генах, однако чаще всего встречаются мутации в генах PMP22, MPZ, GJB1, MFN2. Наследование чаще происходит по аутосомно-доминантному типу, но возможны и другие варианты, в том числе и сцепление с Х-хромосомой.
Патогенетические аспекты болезни Шарко-Мари-Тута и её симптомы
В основе патогенеза болезни Шарко-Мари-Тута лежит повреждение нервов, которое приводит к вторичной мышечной атрофии. Чаще всего страдают «быстрые» двигательные нервные волокна, иннервирующие удаленные мышцы конечностей, берущие на себя большую физическую нагрузку — мышцы стопы и голени. Чуть меньше и позже повреждаются мышцы кистей и предплечий. Также поражаются и чувствительные нервы, что приводит к утрате тактильной, болевой и температурной чувствительности конечностей.
Обычно болезнь Шарко-Мари-Тута манифестирует в возрасте 10–20 лет. Сначала возникает симметричная слабость в ногах, которая приводит к характерному изменению походки по типу степпажа, или, как её еще называют, «петушиной». Затем стопы начинают подворачиваться и деформироваться, увеличивается их свод и образуется полая стопа. По мере прогрессирования атрофии мышц ноги приобретают вид перевернутых бутылок.
Постепенно присоединяется поражение рук: из-за атрофии мышц кисти она становится похожей на лапу обезьяны. Кроме того, страдает чувствительность, в первую очередь поверхностная. Иногда наблюдается цианоз пораженных конечностей и отеки на них.
Болезнь Шарко-Мари-Тута имеет медленное течение. Иногда период между манифестацией и атрофией рук длится 10 лет. Даже несмотря на развившуюся атрофию, пациенты довольно длительное время сохраняют способность к работе и самообслуживанию. При должном уходе продолжительность жизни не страдает и остается на общепопуляционном уровне.
Публикации в СМИ
Болезнь Шарко–Мари–Тута объединяет наследственные сенсомоторные невропатии типов I и II. Заболевание характеризующаяся слабостью и атрофией дистальной группы мышц нижних конечностей и обычно аутосомно-доминантным типом наследования; часто сочетается с другими нейродегенеративными заболеваниями (например, с атаксией Фридрайха).
Генетические аспекты и классификация. Типы и гены: • тип 1A: 118220, PMP22, CMT1A, 601097 (белок 22 миелина), 17p11.2; • тип 1B: 118200, MPZ, CMT1B, 159440, 1q22; • тип 2A: CMT2A, 118210, 1p36 p35; • тип 2B: CMT2B, 600882, 3q13 q22; • тип 2D: CMT2D, 601472, 7p14; • тип 4A: CMT4A, 214400, 8q13 q21.1; • тип 4B: CMT4B, 601382, 11q23; • X сцепленная 1, доминантная: 302800, GJB1, CMTX1, 304040 (ген коннексина CX32, Xq13.1); • X сцепленная 2, рецессивная: CMTX2, 302801, Xp22.2; • демиелинизирующая: CMTND, 601596, 5q23 q33; • с аплазией кожи (302803) • с ладонно-подошвенной кератодермией и дистрофией ногтей (148360) • синдром Коучока (310490) • с атаксией Фридрайха (302900) • с глухотой (118300, 214370) • с тремором (214380) • с птозом и паркинсонизмом (118301)
Патоморфология • Наследственная сенсомоторная невропатия типа I — гистологически определяется сегментарная демиелинизация и ремиелинизация, концентрический рост шванновских клеток (гипертрофическая невропатия) • Наследственная сенсомоторная невропатия типа II — гистологически определяется уоллеровская дегенерация.
Клиническая картина • Наследственная сенсомоторная невропатия типа I •• Начало в среднем детском возрасте •• Слабость разгибателей стопы (свисающая стопа) •• Медленно прогрессирующая атрофия дистальных групп мышц ног (ноги аиста) •• Атрофия мышц кистей развивается позже •• Снижение вибрационной, болевой и температурной чувствительности по типу чулок •• Сухожильные рефлексы снижаются и исчезают •• Утолщённые нервы иногда доступны пальпации •• Аномальное увеличение свода стопы (pes cavus) часто бывает единственным признаком у гетерозиготных носителей дефектного гена •• Течение медленно прогрессирующее, заболевание практически не оказывает влияния на продолжительность жизни • Наследственная сенсомоторная невропатия типа II •• Начало мышечной слабости в возрасте 16–30 лет •• Заболевание прогрессирует медленнее, чем болезнь Шарко–Мари–Тута I типа.
Лабораторные исследования • Болезнь Шарко–Мари–Тута I типа •• Снижение скорости проведения по нервам •• Удлинение дистальной латентности • Болезнь Шарко–Мари–Тута II типа •• Скорость проведения по нервам обычно нормальная •• Снижение амплитуды вызванных потенциалов.
Лечение • Специфическое лечение отсутствует • Выбор профессии должен осуществляться с учётом медленного прогрессирования заболевания • Фиксаторы применяют при свисающей стопе • Ортопедическая коррекция стопы.
Синонимы •• Шарко–Мари мышечная атрофия •• Мышечная атрофия перонеального типа •• Амиотрофия наследственная невральная
МКБ-10 • G60.0 Наследственная моторная и сенсорная невропатия
Классификация болезни Шарко-Мари-Тута
Генетическая классификация очень обширна, поскольку в основе развития заболевания лежат около 40 мутаций, затрагивающих более 20 различных генов. По морфологическим признакам и электромиографическим данным выделяют три основных типа болезни Шарко-Мари-Тута:
- демиелинизирующий тип. Для него характерно разрушение миелиновой оболочки и, как следствие, снижение скорости проведения импульса (СПИ) по срединному нерву;
- аксональный тип. Характерна нормальная или несколько сниженная СПИ по срединному нерву, поскольку в первую очередь страдают аксоны;
- промежуточный тип. Скорость проведения импульса имеет пограничные значения.
Такая классификация имеет смысл для сужения круга поиска при генетической диагностике, поскольку для определенных мутаций характерны свои клинические проявления.
Международная классификация невральной амиотрофии
Ряд патологий с двигательными и чувствительными поражениями относится к группе наследственных амиотрофий. Международная классификация МКБ 10 кодируют нозологию – «G12». Наследственная передача делает невозможным этиологическое лечение. Комплекс распространенных нарушений с глухотой, ретинитом, атаксией лечится поддерживающими препаратами.
Список невральных мышечных амиотрофий:
- Шарко-Мари-Тута;
- Дежерина-Сотта – гипертрофические изменения оболочки нервных волокон обуславливают постепенного нарастание клинических симптомов, обусловленных сенсомоторной невропатией;
- Дегенеративные изменения ствола, рогов спинного мозга возникают при трех клинических формах – поздняя, ранняя, врожденная. Называется нозология «спинальной мышечной атрофией Верднига-Хоффмана»;
- Разрушение моторных нейронов с последовательными атрофическими нарушениями спинномозговых рогов характеризуется мышечными подергиваниями. Называется патология «атрофия Кульберга-Веландера»;
- Другие амиотрофии наследственные – неврогенная злокачественная, лопаточно-малоберцовая, новоанглийская.
Согласно международной классификации болезней следует выделять симптомы с аналогичными клиническими признаками. Родственные проявления лечат по другим схемам, поэтому требуется дифференциальная диагностика.
Варианты синдрома Шарко-Мари-Тута:
- Первый тип сопровождается изменением характеристик передачи нервного сигнала на фоне разрушения миелина оболочек;
- Второй вариант – сохраняется импульсация, но обнаруживается повреждение аксонов швановских клеток.
Согласно википедии нужно верифицировать морфологические формы болезни на ранней стадии до формирования осложнений.
Лечение болезни Шарко-Мари-Тута
Методов излечения болезни Шарко-Мари-Тута на сегодняшний день не разработано. Применяется симптоматическая терапия, направленная на улучшение мышечной трофики. С этой целью назначаются витамины, АТФ, глюкоза, кокарбоксилаза, а также может применяться физиотерапевтическое лечение, ЛФК, массажи. В некоторых случаях необходимо ортопедическое и санаторно-курортное лечение.
В медико-генетическом проводится поиск большинства мутаций, приводящих к развитию болезни Шарко-Мари-Тута. В качестве метода исследования мы применяем секвенирование последовательности ДНК.
Что такое невральная амиотрофия Шарко-Мари-Тута
Хроническое течение болезни сопровождается постепенным прогрессированием мышечных парезов, параличей. Патология сопровождается изменениями мускулатуры с постепенными атрофическими изменениями ног на первоначальном этапе, вторичной атрофией рук. Фасцикулярное подергивание возникает по причине нарушения передачи холинэстеразы нервных волокон по причине инфекционного поражения. Поддерживание лечение направлено на восстановление антиоксидантных, метаболических расстройств.
Уменьшение поступления питательных веществ характеризуется атрофическими изменениями мускулатуры, потерей сократительной функции. Патогенетические механизмы обусловлены разрушением моторных нейронов спинного мозга, стволовых структур, передних внутримозговых рогов.
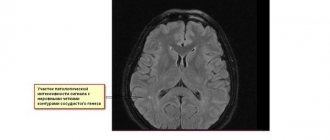
МРТ мультифокальной лейкоэнцефалопатии
Факторы риска и причины ШMT
ШMT является наследственным заболеванием, так что люди, которые имеют близких родственников с заболеванием, имеют более высокий риск развития болезни.
Заболевание поражает периферические нервы. Периферический нервы состоит из двух основных частей: аксона — внутренняя часть нерва и миелиновой оболочки, которая является защитным слоем вокруг аксона. ШМТ может влиять на аксон и миелиновую оболочку.
При ШMT 1
мутируют гены, которые вызывают распад миелиновой оболочки. В конце концов, повреждается аксон, и мышцы пациента больше не получают четких сообщений от мозга. Это приводит к мышечной слабости и потере чувствительности или онемению.
При ШМТ 2
мутирующий ген влияет непосредственно на аксоны. Сигналы передаются не достаточно сильно, чтобы активизировать мышцы и органы чувств, так что пациенты имеют слабые мышцы, плохую чувствительность или онемение.
ШМТ 3
или
болезнь Дежерин-Соттас
, редкий тип заболевания. Повреждение миелиновой оболочки приводит к выраженной мышечной слабости и чувствительности. Симптомы могут быть заметны у детей.
ШМТ 4
является редким заболеванием, которое влияет на миелиновую оболочку. Симптомы обычно появляются в детстве, и пациенты часто нуждаются в инвалидном кресле.
ШМТ Х
вызывается мутацией Х-хромосомы. Она чаще встречается у мужчин. Женщина с CMT X будет иметь очень слабые симптомы.
Как диагностировать ШМТ?
Врач спросит о семейном анамнезе, и выявит признаки мышечной слабости — снижение мышечного тонуса, плоскостопие или высокий свод стоп (кавус).
Для исследования нервной проводимости проводится измерение силы и скорости электрических сигналов, которые проходят через нервы (Электромиография). Электроды помещаются на кожу, и вызывают слабые поражения электрическим током, которые стимулируют нервы. Задержанный или слабый ответ предполагает расстройство нервной системы, и, возможно, ШМТ.
При электромиографии (ЭМГ) тонкую иглу вводят в мышцы. Когда пациент расслабляет или сокращает мышцы, измеряется электрическая активность. Тестирование различных мышц покажет, какая из них страдает.
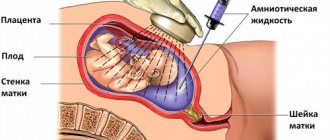
Генетическое тестирование проводится с помощью пробы крови, которая может показать, имеет ли пациент мутации гена.
Симптомы ШМТ у взрослых людей
- Слабость в мышцах ног и лодыжек;
- Искривление пальцев ног;
- Трудности подъема стопы из-за слабых мышц голеностопного сустава;
- Онемение в руках и ногах;
- Изменение формы голени, при этом нога становится очень тонкой ниже колена, в то время как бедра сохраняют нормальный объем мышц и форму (нога аиста);
- Со временем руки ослабевают и пациентам трудно выполнять повседневную работу;
- Появляются боли в мышцах и в суставах, человеку тяжело ходить. Нейропатическая боль возникает вследствие поврежденных нервов;
- В тяжелых случаях пациент может нуждаться в коляске, в то время как другие могут использовать специальная обувь или другие ортопедические устройства.
Клинические симптомы амиотрофии Шарко-Мари-Тута
Изначально слабость локализуется в нижних конечностях. Мышечные подергивания приводят к невозможности нахождения человека на одном месте. Чтобы уменьшить болевой синдром при парестезии пациент начинает топтаться на месте. Покалывание на обеих нижних конечностях не устраняется лекарственными средствами. Двусторонняя атрофия мускулатуры обуславливает специфический вид стопы –«конечности аиста», «симптом перевернутой бутылки». Комплекс изменений обуславливает деформацию нижней конечности. Человек не сможет становиться на пятку. Высокий свод приводит к постоянному поднятию ноги. Ходьба затруднена.
Последовательно присоединяются атрофические изменения со стороны верхних конечностей. Трудности передачи нервного импульса к мелким мышцам руки, симметричная атрофия области гипотенора дополняют диагностический ряд, характерный для нозологической формы. Повышенный тонус мускулатуры обуславливает специфический вид верхних конечностей – «обезьяньи», «когтистые».
Неврологи регистрируют патологию сухожильных рефлексов:
- Ахилловых;
- Коленных;
- Двуглавой мышцы плеча.
К амиотрофическим расстройствам присоединяются чувствительные изменения. Вначале расстраиваются поверхностные рецепторы, формируется синдром «носков и перчаток», при котором утрачивается чувствительность стоп и рук. Одновременно присоединяется гиперемия кожи, гипергидроз конечностей. Повышенная потливость – вторичный симптом, обусловленный утратой иннервации потовых желез. Интеллектуальная функция пациента сохранена.
Амиотрофическая дисфункция Шарко-Мари-Тута сопровождается расстройствами разгибателей и абдукторов стоп. Походка напоминает шаг лошади из-за высокой стопы Фридрейха. Рентгеновский снимок нижних конечностей выявляет молоточковую деформацию пальцев.
Прогрессирование заболевания длительное. От появления первых признаков до атрофии мышц рук проходит около десяти лет. Амиотрофические изменения сопровождаются экзогенными нарушениями.
Провоцирующие факторы болезни:
- Переохлаждение;
- Острая респираторная вирусная инфекция;
- Краснуха;
- Мононуклеоз инфекционный;
- Корь;
- Гиповитаминоз.
Аутосомно-рецессивный или аутосомно-доминантный тип генеалогического анализа, сцепленный с Х-хромосомой позволяет отличить нозологию от миопатического синдрома Говерса-Веландера, бактериального полиневрита, миотонической дистрофии.