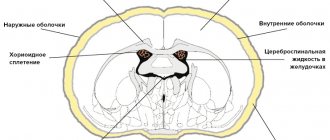
Описание
Синонимы (rus): НМДА-рецептор, НМДАР-аутоиммунный энцефалит
Синонимы (eng): NMDAR-associated autoimmune disorder
Биоматериал: сыворотка/Цереброспинальная жидкость
Показатель(и): Антитела к NDMAR
Метод(и): Реакция непрямой иммунофлюоресценции
Тип контейнера и особенности преаналитики: Стерильный контейнер, БЕЗ добавок, 60 мл; / Биохимическая пробирка с активатором свертывания,6 мл (красная или коричневая крышечка)
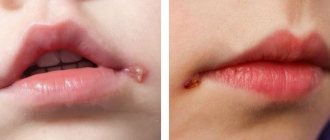
Антитела к NMDA (N-метил-D-аспартат)-глютаматному рецептору относят к семейству «антинейрональных антител», реагирующим с рецепторным аппаратом нейронов, опосредующих межнейрональную передачу сигнала и синаптическую пластичность. Они являются основным маркером «классического» аутоиммунного энцефалита (АЭ) – заболевания, поражающего преимущественно молодых женщин и подростков. Нередко энцефалит имеет паранеопластическую природу и ассоциирован с тератомой яичников и яичек. Заболевание дебютирует с поведенческих расстройств, затем развиваются нарушения сознания и судороги. В ряде случаев отмечается самостоятельно, без связи с опухолью. Выявление антител к NMDA в ликворе является более предподчтительным подходом диагностики аутоиммунного энцефалита.
Анти-NMDA-рецепторный энцефалит
Часть 1: Анти-NMDA-рецепторный энцефалит и шизофрения В поисках причин психических заболеваний ученые доходят до мельчайших структур: речь идет уже не о долях и бороздах головного мозга, а об антителах, ферментах, цитокинах и рецепторах. Что нейромедиаторы и рецепторы к ним вовлечены в генез психических расстройств, мы впервые увидели на примере психотропных препаратов: лечебная практика здесь опередила понимание явления. Только сейчас, когда стали доступны более тонкие методы исследования, ученые начинают разбираться, что же именно было открыто: что происходит с нейромедиаторным обменом и почему. Что заставляет отлаженную медиаторную систему сойти с пути истинного? Один из вариантов ответа — иммунная аутоагрессия. Когда-то считалось, что мозг для иммунной системы недоступен, но в последнее время появляется все больше и больше данных о присутствии иммунных агентов в нервной ткани в норме; конечно, поднимается и вопрос о том, что происходит в патологии, в том числе при психических расстройствах. И действительно, находятся значительные отклонения — термин «нейровоспаление» очень полюбился психиатрам. Внешние агенты, как причина таких нарушений исключаются в первую очередь, оно может быть только иммунным; остается вопрос: не воспаление ли это приводит к дисфункции нейромедиаторной системы, которую корректируют психотропными препаратами. Если это так, существующий подход к лечению психических расстройств неверен: терапия должна быть в первую очередь направлена на иммунную систему. Такое уже практикуется: например, в схемы лечения шизофрении и депрессивных эпизодов добавляют НПВС — и получают неплохой эффект. В этом случае достаточно только обнаружить структуры, которые попали под огонь собственной иммунной системы, и загадка психических расстройств решена. Мы знаем, что патогенез должен вовлекать какое-то из звеньев нейромедиаторного обмена (почему бы и не рецептор) и имеется аутоиммунное воспаление, которое как раз может его затрагивать. Поэтому так много эмоций вызвало описание анти-NMDA-рецепторного энцефалита (анти-NMDAR-энцефалит): клиника психотического расстройства, которое невозможно отличить от шизофрении, антитела к NMDA-рецепторам — кажется, мы начали что-то понимать. Но как всегда все оказалось не так просто. Анти-NMDAR-энцефалит был впервые описан не так давно, в 2007 году. Впервые зарегистрирована была достаточно однородная группа пациентов: молодые женщины с тератомой яичника, у которых развилось психотическое состояние, затем на его фоне неврологические нарушения, в первую очередь двигательные. Неврологическая симптоматика была совершенно полиморфной: экстрапирамидные гиперкинезы и эпилептические припадки, расстройства сна, вегетативные проявления, нарушения сознания вплоть до комы. Психопатологические же симптомы сохранялись на протяжении всей болезни вне зависимости от тяжести неврологических (за исключением периодов утраты сознания) и соответствовали клинике шизофрении вплоть до люцидных кататонических эпизодов; именно эти симптомы появлялись первыми, и большинство пациентов первоначально попали на прием к психиатру.
Неврологические симптомы очень быстро прогрессировали (в течение нескольких месяцев) и нередко грозили летальным исходом, но с удалением опухоли практически сразу же разрешались — заболевание было расценено как паранеопластическое. Впрочем, впоследствии выяснилось, что оно может рецидивировать; после успешного лечения в полной ремиссии проходило от 3 месяцев до 6 лет. Внимательные клиницисты расспросили больных, как начиналось заболевание — четверть рассказывала, что незадолго до развития первых симптомов перенесли что-то похожее на вирусное заболевание (катар верхних дыхательных путей, лихорадка, головная боль). Из антител к бактериальным антигенам выявляли противомикоплазменные иммуноглобулины, АСЛ-О; 1 пациентка незадолго до развития симптомов была вакцинирована АКДС. Здесь некоторые врачи вспомнили летаргический энцефалит: та же полиморфная картина неврологических и психиатрических расстройств после напоминающего инфекцию продромального периода. Поскольку сам летаргический энцефалитостается загадкой, подтвердить или опровергнуть эту гипотезу невозможно; но, например, характерного постэнцефалитического паркинсонизма у таких пациентов не отмечали. Кроме летаргического энцефалита связь с повышением титра анти-NMDA-рецепторных антител обнаружили при энцефалите Хашимото и PANDAS-синдроме, также аутоиммунных. Исследователи заинтересовались NMDA-рецепторами и антителами к ним, которые служили критерием диагностики заболевания. Хотя оно и было достаточно редким, собрав больше случаев, врачи увидели, что, во-первых, не всегда симптоматика развивается на фоне опухолевого заболевания (и не только на фоне тератомы, если оно все же есть). А во-вторых, особенно когда она сравнительно легкая, то, если неврологические нарушения не доводят пациента до реанимации или вовсе отсутствуют (в то время как психиатрические присутствовали всегда), диагностика представляет большие трудности: практически невозможно заподозрить у пациента аутоиммунный энцефалит, а рутинно выявление антител проводить никто не будет. Логично предположить, что у какого-то количества пациентов, наблюдающихся у психиатров и неврологов с совершенно другими диагнозами, анализ даст положительный результат. А что если у всех? Исследовали пациентов с шизофренией. О шизофреноподобных психотических симптомах при временной фармакологической блокаде NMDA-рецепторов у здоровых добровольцев ранее сообщали, и этот механизм рассматривался как потенциальное объяснение генеза шизофрении; но доказать его как основной, да еще и увидеть причину было бы прорывом. На деле же антитела к NMDA-рецептору обнаружились у совсем небольшого количества пациентов с диагнозом «шизофрения» по критериям DSM-IV: наибольший процент в исследовании составил 6,5%, а по данным мета-анализа и вовсе 1,49%. Говорить о том, что причина шизофрении в аутоиммунной агрессии против NMDA-рецепторов, нельзя, но одновременно возникает вопрос, как объяснить фармакологические и генетические данные, подтверждающие роль этих рецепторов. Но нельзя и отбросить тот небольшой процент пациентов, у которых антитела были обнаружены — по всей видимости, им необходимо лечение в соответствии с принципами терапии аутоиммунных заболеваний. Кроме того, поскольку для пациентов с анти-NMDAR-энцефалитом характерны опухолевые процессы, а также аутоиммунные, как выяснилось в ходе дальнейших исследований, заболевания, пациентов с положительными результатами необходимо дальше обследовать в соматической клинике для их исключения. Как и следовало ожидать, патогенез шизофрении все же сложнее, чем повреждение одного-единственного типа глутаматных рецепторов, но и оно имеет место. Что происходит с большинством больных шизофренией на нейромедиаторном уровне — какие-то другие нарушения в обмене глутамата, может, тоже аутоиммунные? Ту же симптоматику дают нарушения в других нейромедиаторных системах? А может, шизофрения вовсе не является физиологически и биохимически однородным заболеванием, и у разных пациентов симптомы связаны с разнородными нарушениями нейромедиаторного обмена? Основываясь только на психопродукции, врачу было бы затруднительно оценить, находится пациент под действием ЛСД, действующего на серотониновые рецепторы, или, например, антихолинергического препарата. Возможно, в той же ситуации находится психиатр, когда видит разных больных шизофренией. Специфические черты галлюцинаторных образов для каждого механизма действия наркотического препарата можно выделить, сосредоточившись на различиях и точно зная, о каком препарате речь идет в каждом случае, но врач-психиатр работает иначе. Содержание образов его мало интересует, и критерии, по которым ставится диагноз, не позволяют остановиться на этих различиях. Поэтому важная возможность, которую дает нам анти-NMDAR-энцефалит — попробовать выделить группу, природа нарушений у которой более-менее ясна, из остальной массы больных, и точнее проследить корреляцию между «физиологией» и «феноменологией». Очевидная же цель выделения — обеспечить таким больным адекватное лечение, действующее именно на аутоиммунный процесс. Хотя, обращаясь к сказанному выше о возможном нейровоспалении (пусть и не всегда в отношении NMDAR) у подавляющей части больных и уже имеющейся практике назначения НПВС в дополнение к антипсихотикам, возможно, пациентом с антителами к NMDA-рецепторам при диагнозе «шизофрения» всего лишь повезло раньше перейти к лечению, которое эффективно для всех больных с таким диагнозом. В плане лечения анти-NMDA-рецепторный энцефалит не представляет таких трудностей, как с диагностикой. Небольшое количество пациентов (около 2%) полностью излечило удаление опухоли, которая спровоцировала аутоиммунный процесс. Большинству пациентов, имевших опухоль, кроме операции понадобилось лечение препаратами, влияющими на иммунную систему, то же самое относилось и к пациентам, у которых опухоль не обнаружили. В первую линию иммунотерапии входили стероиды и внутривенные иммуноглобулины, у меньшего количества пациентов (соответственно тяжести состояния) применили плазмаферез. Значительное улучшение состояния наступило у половины получавших такое лечение в течение четырех недель. Оставшиеся разделились на две группы: первую продолжали лечить теми же препаратами или совсем прекращали, вторая перешла на терапию второй линии. В это понятие входило применение ритуксимаба и циклофосфамида; среди получавших эти препараты 78% на осмотре через 2 года были практически здоровы; среди тех, кто продолжал принимать терапию первой линии или прекратил лечение, процент выздоровевших составил через 2 года 55%. В целом можно говорить о достаточно высокой вероятности регрессии симптомов со временем даже при отсутствии и малоэффективности лечения. За двухлетний период наблюдения рецидив случился у 12% пациентов, в основном у тех, чье заболевание не было связано с опухолевым процессом. Больше половины всех обострений отличались меньшей тяжестью, чем первый эпизод заболевания, вероятность и тяжесть обострения значительно снижала проведенная иммунотерапия. Но при имеющейся клинической картине необходимость именно такого лечения неочевидна: приводят данные, что 77% пациентов первоначально лечатся у психиатра, и мишенью лечения становится отнюдь не иммунная система. Если какой-то небольшой процент таких пациентов есть в практике каждого психиатра, и они ведутся с диагнозом «шизофрения», будут ли они как-то отличаться от других пациентов по отношению к психофармакологической терапии? Есть опыт применения практически всех видов антипсихотиков при анти-NMDAR-энцефалите; особенности касаются не столько их эффективности, сколько побочных эффектов. Во-первых, энцефалит сам по себе может вызывать экстрапирамидную симптоматику. Мало того, что назначение типичных антипсихотиков увеличивает вероятность ее развития и тяжесть; если такие симптомы появятся после назначения классического нейролептика пациенту с психозом, они будут истрактованы именно как побочное действие нейролептика и затруднят диагностику аутоиммунного энцефалита. Во-вторых, при злокачественном нейролептическом синдроме (ЗНС) антитела к NMDAR продуцируются даже у тех пациентов, которые раньше их не имели; по всей видимости, аутоиммунная агрессия против NMDA-рецепторов — это также и один из элементов патогенеза ЗНС как самостоятельной патологии. За счет уже имеющегося поражения NMDAR ЗНС у таких пациентов будет протекать еще тяжелее, но, с другой стороны, может привести к гипердиагностике анти-NMDAR-энцефалита. Среди нарушений настроения у пациентов с этой разновидностью антирецепторного энцефалита преобладают мании. Описано применение и вальпроевой кислоты, и препаратов лития, но, учитывая возможность судорог и сопутствующие нарушения сна, авторы обзора по психофармакологии анти-NMDA-рецепторного энцефалита рекомендуют бензодиазепины, в том числе внутривенно. Их также рекомендуют, если у пациента развивается кататония. Назначение антипсихотиков здесь опасно, поскольку с большей вероятностью развивается ЗНС: кататония тоже относится к состояниям, сопровождающимся повышением титра антител к NMDA-рецепторам. Противоречивая мера — применение электросудорожной терапии (ЭСТ). Патогенетически оно обосновано, поскольку имеются данные, что после применения ЭСТ в нервной ткани повышается содержание мРНК субъединиц NMDA-рецептора, что способствовало бы их восстановлению. С другой стороны, сообщают, что, купировав таким образом приступ кататонии, врач получает в дальнейшем более резистентный психоз. Никаких существенных отличий от пациентов с шизофренией в реакции на психофармакотерапию не обнаружили; при отсутствии данных о природе заболевания они получали бы ту же терапию, что и другие больные c психотическими симптомами, еще очень долго. Но впечатляют данные о результатах иммунотерапии: в ближайшие два года после постановки диагноза у большинства пациентов удалось добиться практически полного регресса симптоматики, а если заболевание и рецидивировало, как правило, это был один-единственный эпизод, намного менее тяжелый по сравнению с тем, что психиатры долго и безуспешно лечили раньше. Речь, конечно, идет о казуистических случаях, но, возможно, из таких и состоит диагноз шизофрении. Даже если это один процент, немаловажно, что в течение двух лет пациента можно, как мечтают психиатры, вернуть обществу, — и что интересующиеся патогенезом шизофрении ученые могут спать на один процент спокойнее.
Антирецепторные энцефалиты достаточно редки: в развитых странах (где вообще есть возможность их диагностировать) распространенность составляет всего 5–10 на 100 тысяч человек. “Находить” их стали недавно, в начале этого десятилетия; в основном исследование на антирецепторные антитела проводят пациентам с неясной этиологией заболевания или в исследовательских целях. За высокой стоимостью такой анализ просто не назначают, если сомнений в диагнозе нет. Однако, во-первых, эти данные могли бы открыть нам новые грани патогенеза давно известных болезней, а во-вторых, поскольку эта группа заболеваний новая и мало изучена, врачи легко могут уложить симптомы, которые видят, в рамки уже давно известных заболеваний, а полное представление о том, насколько часто в действительности нужно проверить уровень антител к рецепторам, не сложилось пока даже у ученых. Из того, что известно на сегодняшний день, для всех антирецепторных энцефалитов характерны общие черты (которые явно прослеживаются на примере анти-NMDA-рецепторного энцефалита):
- психиатрическая и неврологическая симптоматика,
- часто — связь с опухолями или предрасположенность к аутоиммунным заболеваниям,
- хороший ответ на иммунотерапию,
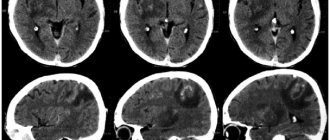
- из диагностических признаков: у части пациентов лимфоцитарный плеоцитоз в анализе ликвора и аномальные результаты МРТ (именно эти показатели часто заставляют усомниться в прежнем неврологическом или психиатрическом диагнозе — если до них доходит дело).
Часть 2: Дебри антител В первой части мы уже отметили, чем такие заболевания действительно интересны: возможностью соотнести клинику с таким узким, затрагивающим всего один тип рецепторов, поражением. Анти-NMDAR-энцефалит — наиболее известный из всех заболеваний этой группы, но, коль скоро нас интересует патогенез, нужно сказать и о более редких поражениях рецепторов. 1) Анти-GABA-B-рецепторный энцефалит Впервые был описан в 2010 году и редок даже среди антирецепторных энцефалитов — на него приходится 5% среди всех заболеваний этой группы. Проявляется симптомами лимбического энцефалита: амнезия, спутанность сознания и выраженный судорожный синдром — как правило, вторично-генерализованные судороги с источником в лобной доле. Редко заболевание начинается с атаксии или опсоклонус-миоклонус синдрома, но всегда прогрессирует до лимбического энцефалита. Наиболее часто развивается у пожилых пациентов с мелкоклеточным раком легких (такой диагноз имеет 50% с анти-GABA-B-рецепторным энцефалитом, причем проявления энцефалита могут предшествовать обнаружению рака). На МРТ — одно- или двустороннее поражение височных долей. Помимо антител к GABA-B, могут присутствовать антитела, отражающие тенденцию к аутоиммуному процессу или наличие опухоли. Кроме антирецепторного лимбический энцефалит может быть паранеопластическим — возможных причин его развития всего две. В случае паранеопластического заболевания речь идет тоже о формировании антител, но уже не к рецепторам, а чаще к внутриклеточным антигенам. Есть и поверхностно расположенные антигены, к которым могут сформироваться антитела в рамках паранеопластической реакции, — VGPC, белки потенциалзависимых калиевых каналов. Такой паранеопластический процесс особенно характерен для пациентов с мелкоклеточным раком легких; высока вероятность обнаружить у пациента оба типа антител, поэтому определить, какие симптомы на счет какой аутоиммунной реакции отнести, практически невозможно. Иммунотерапия дает у таких пациентов очень хорошие результаты: частично или полностью восстанавливаются 75% пациентов. В большой степени исход зависит от лечения первичной опухоли, если она есть, и ухода на пике выраженности неврологических симптомов. 2) Анти-GABA-A-рецепторный энцефалит На данный момент был зарегистрирован всего у 6 пациентов: 2 маленьких ребенка, 1 подросток и 3 взрослых от 23 до 68 лет. Проявлялся эпилептическим статусом, который не поддавался никакому лечению и потребовал введения в искусственную кому. Отклонения в анализе ликвора были у 5 из 6 пациентов, у всех разные: плеоцитоз, протеиноз, олигоклональные антитела. Из всех энцефалитов этот характеризуется наиболее выраженными изменениями на МРТ: затронуты не только височные доли, как это обычно бывает; имеются мультифокальные корковые и подкорковые очаги. Еще одна особенность состояла в том, что опухолевых заболеваний у большинства пациентов не было — только у одного в анамнезе ходжкинская лимфома. Иммунотерапию получала половина пациентов, и она дала хороший результат. У одного интенсивность симптомов со временем уменьшилась без иммунотерапии, однако сохранился эпилептический синдром. Иммунный профиль пациентов, хотя и послужил основанием для постановки такого диагноза, достаточно сложен. У большинства пациентов кроме анти-GABA-A обнаружили антитела к GAD (антитела к глутаматдекарбоксилазе, основному антигену бета-клеток поджелудочной железы; они выявляются, например, у большинства больных сахарным диабетом 1 типа) и TPO (тиреоидная пероксидаза, антитела к ней — маркер аутоиммунных заболеваний щитовидной железы). Были описаны случаи возникновения лимбического энцефалита с судорогами на фоне высокого титра антител к GAD-65 — следует ли их после появления таких данных квалифицировать как анти-GABA-A-рецепторный энцефалит, или наоборот? Та же проблема возникает с так называемым энцефалитом Хашимото, ассоциированным с высоким титром антител к TPO. Дополнительно у 12 пациентов были обнаружены антитела к GABA-A, но в более низких титрах. Спектр симптомов у них был шире: у 2 — опсоклонус-миоклонус синдром, у 4 — синдром ригидного человека, у 6 — энцефалит с судорогами меньшей тяжести. 3) Анти-AMPA-рецепторный энцефалит Кроме NMDA-рецепторов жертвой аутоиммунной агрессии могут также стать AMPA-рецепторы к глутамату. Проявлением ее становится, как при большинстве антирецепторных процессов, лимбический энцефалит, но особенностью здесь является (также как и при анти-NMDAR-рецепторном энцефалите) большая выраженность психиатрических симптомов. Судороги, наоборот, встречаются реже, у менее чем у половины пациентов. По данным исследований — также лимфоцитарный плеоцитоз, на МРТ — поражение медиальных отделов лобных долей. Чаще страдали пожилые женщины, у 70% выявлялись опухоли (легких, тимуса, молочной железы). 50% имели в анамнезе аутоиммуные заболевания: тиреоидит, сахарный диабет 1 типа, синдром Рейно или синдром ригидного человека. Их наличие, по всей видимости, серьезно ухудшает прогноз. По клинике собственно анти-AMPA-рецепторный энцефалит неотличим от анти-NMDA-рецепторного, это можно объяснить функциональной общностью рецепторов. Однако у трети пациентов выявлялись также антитела к другим протеинам нервной ткани, и во всех случаях развивался синдром, более характерный именно для этого, другого аутоиммунного поражения. Это вызывает вопрос о специфичности антител к AMPAR: возможно, они могут быть вторичными для других аутоиммунных поражений и собственную симптоматику давать в меньшей степени, но возможна и обратная ситуация, когда специфичность процессу придает именно агрессия против AMPA-рецепторов. 4) mGluR5 и mGluR1 Кроме ионотропных AMPA- и NMDA-, есть метаботропные рецепторы к глутамату, которые тоже могут стать мишенью аутоиммунной агрессии. Известно сочетание лимфомы Ходжкина с лимбическим энцефалитом, обусловленным выработкой антител к mGluR5 — синдром Офелии. Назван так, поскольку на фоне лимбического энцефалита при этом расстройстве высока вероятность развития делирия. С 1982 года, когда синдром был описан впервые, всего зарегистрировали 5 таких случаев. На фоне ходжкинской лимофмы также может развиться мозжечковая атаксия, уже в результате поражения mGluR1 рецептора. 5) Анти-глицин-рецепторный энцефалит Наиболее частым проявлением этого энцефалита был синдром ригидного человека и наиболее его выраженная форма — PERM синдром (прогрессирующий энцефаломиелит с ригидностью и миоклонусом). Для синдрома ригидного человека характерны:
- Собственно ригидность с преобладанием тонуса в мышцах туловища и проксимальных мышцах конечностей, а также в разгибателях над сгибателями, из-за чего пациент находится в характерной позе с запрокинутой головой, развернутыми плечами, резко выпрямленной или прогнувшейся в пояснице спиной; повышение тонуса может сопровождаться или не сопровождаться гиперрефлексией;
- Миоклонус;
- Вегетативные расстройства;
- Резкое повышение мышечного тонуса и спазмы в ответ на раздражение — так называемая гиперэкплексия, или стартл-синдром.
При PERM синдроме присоединяются симптомы энцефаломиелита, наиболее характерны разнообразные поражения ствола, судороги и атаксия. В самом большом исследовании пациентов с антителами к рецептору глицина, которое включало 42 человека, такой диагноз был поставлен 33 пациентам. МРТ у большинства пациентов была не показательна, у отдельных пациентов выявлялось поражение теменных долей или, чаще, очаги разной протяженности в спинном мозге. Наиболее частое изменения СМЖ — как и в предыдущих случаях, лимфоцитарный плеоцитоз. Этот антирецепторный энцефалит оказался менее остальных ассоциирован с опухолевыми заболеваниями, однако у двух пациенток, имевших в анамнезе опухоль (тимому и лимофму Ходжкина), PERM-синдром сочетался с миастеноподобной мышечной слабостью и миоклонусом в ответ на раздражение (в то время как обычный PERM характеризуется лишь повышением тонуса).
Раньше считалось, что синдром ригидного человека и PERM-синдром обусловлены аутоиммунной агрессией против GAD-65, о которой говорилось выше в связи с лимбическим энцефалитом. У троих пациентов в проспективном исследовании и в еще большем количестве случаев ретроспективно антитела к глициновому рецептору и к GAD обнаруживались одновременно, и здесь уместен тот же вопрос, что и с анти-AMPA-рецепторным энцефалитом: неважных белков в ткани нет, и любое аутоиммунное поражение будет иметь патофизиологические последствия, но в некоторых случаях уровня, который видят врачи, изменения достигают только при сочетании нескольких антирецепторных процессов. Один из них может быть предрасполагающим, а другой — придающим специфичность и определяющим клинику, но что за чем следует и что какие симптомы обусловливает, мы только начинаем разбираться. Ранее при синдроме ригидного человека и PERM обнаруживали только GAD-65, теперь выявили группу пациентов, у которых обнаруживаются только антитела к глициновому рецептору, но есть и группа, где два аутоиммуных процесса пересекаются, а возможно, впоследствии будут обнаружены новые антитела, общие для всех трех групп. 6) Анти-D2-рецепторный энцефалит Дофаминовый рецептор 2 типа — D2 рецептор — широко известен как мишень типичных антипсихотиков; к психотическим расстройствам он имеет непосредственное отношение — как и к контролю движений, расстройство которых мы наблюдаем при лечении классическими нейролептиками. Поскольку поражение именно базальных ганглиев имеет достаточно специфическую клинику, здесь ученые “знали, где искать”, и антитела к этому рецептору обнаружили при ревматической хорее Сиденгама и синдроме Туретта. Под вопросом остаются психотические расстройства: как и в случае анти-NMDAR-энцефалита, возможно, какая-то часть пациентов с психиатрическим диагнозом имеет антирецепторные антитела и подлежит иммунотерапии. Таких исследований пока недостаточно, однако по уже имеющимся данным среди детей с первым психотическим эпизодом (аутоиммунные заболевания, если не являются паранеопластическими, что пока не было замечено для анти-D2-энцефалита, обычно манифестируют достаточно рано, поэтому объектом исследования стали дети) пациентов с высокими титрами к D2 рецептору даже больше, чем к NMDAR. Антитела могут вырабатываться не только к субъединицам рецепторов, но и ко многим другим белкам нервной ткани. В отличие от некоторых генетических заболеваний, где дефект может быть точечным и все патологические процессы становятся его ответвлениями, здесь многие структуры повреждаются одновременно: если дефект иммунной системы предрасполагает ее к аутоагрессии в целом, неразумно рассчитывать, что поврежден только один тип рецепторов, антитела к которому мы нашли. Большинство приведенных “диагнозов” антирецепторных энцефалитов — конструкты недавние, но и прожить им предстоит недолго. Пересечения между ними находят уже сейчас, а с расширением наших знаний и диагностических возможностей будут обнаруживать все больше разных проявлений аутоиммунной агрессии. Набор клинических симптомов, который сейчас приписывают поражению одного рецептора, перейдет в руки целой группы; какие-то симптомы из него исчезнут, то, что сейчас — один из нескольких случаев, в последствии окажется статистически незначимой редкостью для этого синдрома.
С одной стороны, сегодняшние данные по антирецепторным энцефалитам дают нам повод поразмыслить о соотношении клиники и тончайшей патофизиологии; с другой стороны, эта область — пример того, как быстро могут поменяться названия и представления в медицинской науке, когда на первой линии ее фронта совершаются новые открытия. Источники
- https://vk.cc/7qenjL Graus F. et al. A clinical approach to diagnosis of autoimmune encephalitis //The Lancet Neurology. – 2016. – Т. 15. – №. 4. – С. 391-404.
- https://vk.cc/7qfsdk Kim T. J. et al. Clinical manifestations and outcomes of the treatment of patients with GABA B encephalitis //Journal of neuroimmunology. – 2014. – Т. 270. – №. 1. – С. 45-50.
- https://vk.cc/7qfIOW Hirsch L. J. A new encephalitis with GABAA receptor antibodies //The Lancet Neurology. – 2014. – Т. 13. – №. 3. – С. 239-240.
- https://vk.cc/7qfMiK Widman G. et al. Treating a GAD65 antibody-associated limbic encephalitis with basiliximab: a case study //Frontiers in neurology. – 2015. – Т. 6.
- https://goo.gl/ope9Ja Carvajal-González A. et al. Glycine receptor antibodies in PERM and related syndromes: characteristics, clinical features and outcomes //Brain. – 2014. – Т. 137. – №. 8. – С. 2178-2192.
- https://goo.gl/4osQtK Höftberger R. et al. Encephalitis and AMPA receptor antibodies Novel findings in a case series of 22 patients //Neurology. – 2015. – Т. 84. – №. 24. – С. 2403-2412.
- https://goo.gl/2vR9HB Pathmanandavel K. et al. Antibodies to surface dopamine-2 receptor and N-methyl-D-aspartate receptor in the first episode of acute psychosis in children //Biological psychiatry. – 2015. – Т. 77. – №. 6. – С. 537-547.
- Nitta M. et al. Adjunctive use of nonsteroidal anti-inflammatory drugs for schizophrenia: a meta-analytic investigation of randomized controlled trials //Schizophrenia bulletin. – 2013. – Т. 39. – №. 6. – С. 1230-1241. https://vk.cc/7mddx4
- Köhler O. et al. Effect of anti-inflammatory treatment on depression, depressive symptoms, and adverse effects: a systematic review and meta-analysis of randomized clinical trials //JAMA psychiatry. – 2014. – Т. 71. – №. 12. – С. 1381-1391. https://vk.cc/7mde3p
- Lennox B. R., Coles A. J., Vincent A. Antibody-mediated encephalitis: a treatable cause of schizophrenia. – 2012. https://vk.cc/7me2LH
- Pollak T. A. et al. Prevalence of anti-N-methyl-D-aspartate (NMDA) receptor antibodies in patients with schizophrenia and related psychoses: a systematic review and meta-analysis //Psychological medicine. – 2014. – Т. 44. – №. 12. – С. 2475-2487. https://vk.cc/7mfdNL
- Irani S. R. et al. N-methyl-D-aspartate antibody encephalitis: temporal progression of clinical and paraclinical observations in a predominantly non-paraneoplastic disorder of both sexes //Brain. – 2010. – Т. 133. – №. 6. – С. 1655-1667. https://vk.cc/7mfux5
- Titulaer M. J. et al. Treatment and prognostic factors for long-term outcome in patients with anti-NMDA receptor encephalitis: an observational cohort study //The Lancet Neurology. – 2013. – Т. 12. – №. 2. – С. 157-165. https://vk.cc/7mupq3
- Kuppuswamy P. S., Takala C. R., Sola C. L. Management of psychiatric symptoms in anti-NMDAR encephalitis: a case series, literature review and future directions //General hospital psychiatry. – 2014. – Т. 36. – №. 4. – С. 388-391. https://vk.cc/7mvsv8
Интерпретация
Отрицательный результат выявления антител к NMDA–рецептору в ликворе значительно снижает клиническую вероятность наличия аутоиммунного энцефалита. Клиническими проявлениями NMDA-энцефалита служат симптомы возбужденного поведения, паранойи, психоза, нарушения памяти и речи, судороги. Выявление антител в цереброспинальной жидкости является более чувствительным методом по сравнению с исследованием сыворотки. Показатели чувствительности и специфичности близки к 100%. При наличии характерных симптомов заболевания и отрицательном результате на наличие NMDA антител, может быть рекомендовано исследование на антитела к вольтаж-зависимым калиевым каналам (VGKC), в частности антител к LGI-1 и CASPR. Титр антител в цереброспинальной жидкости лучше коррелирует с рецидивами заболевания, чем в сыворотке. Кроме того, у пациентов с благоприятным исходом болезни наблюдается более быстрое и большее снижение уровня антител в цереброспинальной жидкости, чем у пациентов с неблагоприятным исходом.
Использованная литература
- Суровцева, А.В., Скрипченко, Н.В., Иванова, Г.П. и др. Энцефалит с антителами к NMDA-рецепторам. Рос вестнперинатол и педиат., 2014. — № 6.
- Богадельников, И.В., Бобрышева, А.В., Вяльцева, Ю.В. и др. Энцефалит, вызванный антителами к NMDA-рецепторам нейронов. ЗР, 2013. — № 3(46).
- Kasper, D., Fauci, A., Hauseret, S. Harrison`s Principles of Internal Medicine 19/E (Vol.1). McGraw-HillEducation, 2015.
- Струков, А.И., Серов, В.В. Патологическая анатомия: учебник. — М. : Литтерра, 2010. — 848 с.
- Guasp, M., Dalmau, J. Encephalitis associated with antibodies against the NMDA receptor. Med Clin (Barc), 2021. — Vol. 151(2). — P. 71-79.
Аутоиммунные заболевания
Существует также группа энцефалитов, которые вызываются аутоиммунными процессами в организме. В этом случае собственные иммунные клетки больного начинают атаковать головной мозг. Заболевания такого характера крайне тяжело поддаются лечению, вызывают слабоумие, приводят к нарушениям мозговой деятельности и работы периферической нервной системы. Помимо деменции, болезнь сопровождается параличом и припадками, похожими на эпилептические. К заболеваниям такого рода относят, например, лимбический энцефалит. Болезнь вызывает аутоиммунный отклик организма на присутствие раковых клеток или заболевание, имеющее инфекционную или вирусную природу. Скорость развития лимбического энцефалита делит болезнь на острый и подострый вид. Причины анти-рецепторного энцефалита рассмотрим ниже.
Что такое энцефалит?
Энцефалиты вызывают различные патологические нарушения в организме и приводят к формированию деменции (слабоумия). Болезнь может поражать не только мозг, но и часть внутренних органов и суставов.
Патологические состояния могут быть вызваны рядом причин. По факторам, провоцирующим заболевание, различают следующие виды энцефалитов:
- воспаление, вызванное инфекцией;
- бактериальный или грибковый энцефалит;
- заболевание, спровоцированное воздействием на организм токсического вещества;
- аутоиммунные энцефалиты.
Болезнь влияет на разные участки мозга. Воспаление может быть локализовано в его коре, подкорке или мозжечке. Каждый тип отличается своими собственными признаками, симптомами и методами лечения.
Что же такое анти-рецепторный энцефалит? Об этом далее.
Культура и общество
Симптомы анти-NMDA-рецепторного энцефалита легли в основу многих художественных произведений о вселении демонов в человека. Поскольку клинические проявления болезни довольно разнообразны, ее долго не могли выделить в отдельную группу патологий.
Известный репортер из Нью-Йорка Сюзанно Кахалан издала книгу «Мозг в огне: мой месяц безумия». Впоследствии произведение стало бестселлером. Журналистка рассказывает о том, как долго не могли определить ее заболевание, и каким образом проходило лечение с реабилитацией. Стоимость медицинских процедур составила 1 млн. долларов.
Lineman Amobi Okoye, защитник команды по американскому футболу Dallas Cowboys, лечился от энцефалита 17 месяцев, включая 3 месяца комы, вызванной врачами для поддержания стабильного состояния. После выздоровления футболист вновь вернулся к профессиональному спорту.
Острый синдром
При остром синдроме, развитие болезни происходит стремительно на протяжении трех-пяти дней. Если не принять срочные меры, то смерть наступает очень быстро. При подостром течении заболевания первые признаки становятся заметны по истечении нескольких недель от начального момента развития патологии. Эти состояния характеризуются следующими симптомами:
- нарушением памяти;
- когнитивными расстройствами;
- эпилептическими припадками;
- психическими нарушениями (высокий уровень тревожности, депрессивные состояния, возбуждение);
- поведенческими расстройствами.
Кроме того, явными признаками являются: прогрессирующее слабоумие, нарушения сна, эпилептические припадки с галлюцинациями. Весьма нередки случаи, когда аутоиммунные поражения мозга соотносят с наличием раковых заболеваний. Как правило, такой энцефалит вызывается раком легких.
Возможные осложнения
Аутоиммунные заболевания сложны для диагностики, поэтому при отсутствии надлежащего опыта у врача, пациент может оказаться в психиатрической клинике из-за неправильно поставленного диагноза. Отсутствие необходимого лечения приводит к психиатрическим отклонениям, которые зачастую бывают необратимы. Кроме того, есть большая вероятность, что пациент может впасть в кому. Если больной не принимает необходимые для лечения медикаменты, очень быстро развивается вегетативное состояние, а у трети пациентов наступает летальный исход.
Последствия
Последствия перенесенного анти-NMDA-рецепторного энцефалита отражаются на состоянии познавательной сферы. В ряде случаев в период реабилитации придется заново учиться ходить и владеть своим телом. Иногда больные непроизвольно совершают движения руками.
К опасным последствиям относят потерю чувствительности определенных рецепторов (голода, жажды). Больной может подолгу не есть и не пить, что повышает риск ухудшения его состояния. Потеря чувствительности кожи грозит ожогами и различными травмами.
Память пациента ухудшается. Некоторые люди не помнят событий, случившихся раньше, чем неделю назад. Во время реабилитации и после выздоровления больному приходится принимать большой объем медикаментов.
К осложнениям относят прогрессирующую деменцию (слабоумие). Однако она развивается не во всех случаях.
Около 50% больных выздоравливают полностью. Треть пациентов имеет незначительные остаточные явления. По статистическим данным 10% случаев болезни оканчиваются летально. При нахождении опухоли на начальном этапе развития функции организма восстанавливаются полностью. Шанс на благоприятный исход увеличивается, если обратиться к врачу при первых симптома.
Инфекционные и бактериальные воспаления
Факторами, вызывающими инфекционный энцефалит, являются вирусы и бактерии. Например, вирус герпеса, ВИЧ-инфекция, энцефалитный вирус, туберкулезные бактерии, стрептококк и стафилококк, токсоплазма. Кроме того, серьезной проблемой является клещевой энцефалит. Это вирусное заболевание, разносчиком которого являются некоторые виды клещей. Вирус попадает в организм после укуса насекомого.
Однако при клещевом энцефалите головной мозг поражается не всегда, в 50 % случаев пациент испытывает только лихорадку. К вирусным видам относится и японский энцефалит. Болезнь очень опасна и в большинстве случаев заканчивается смертельным исходом. Для этого вида энцефалита характерно быстрое течение, через несколько дней после заражения больной впадает в кому. Герпесный энцефалит смертелен в девяти из десяти случаев, он практически не поддается лечению.
Как проявляется анти-рецепторный энцефалит? Расскажем поподробнее.