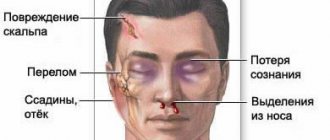
Клинические синдромы и симптомы ишемического инсульта в бассейне задней мозговой артерии
Локализация атероматозного поражения в задней мозговой артерии или в начале одной из её ветвей, а также степень сужения обычно определяют начало, тяжесть течения и характер клинического синдрома. Значительную, но менее важную роль играют и другие факторы, включая коллатеральный кровоток через заднюю соединительную артерию или кортикальные ветви и вязкость крови. Однако даже при наличии атеросклеротической бляшки в задней мозговой артерии механизмом, ответственным за развитие инсульта, обычно служит эмболическая окклюзия этой артерии или её ветвей.
Изменения задней мозговой артерии обусловливают появление синдромов, которые делятся на две группы:
- Синдромы поражения среднего мозга, субталамуса и таламуса, связанные с атеросклеротическим сужением, атеросклеротической или эмболической закупоркой проксимального прекоммунального сегмента задней мозговой артерии или начала её пенетрируюших ветвей
- Синдромы, поражения коры, вызванные атеросклеротическим сужением, атеротромботической или эмболической окклюзией посткоммунального сегмента задней мозговой артерии
Проксимальные прекоммунальные синдромы (центральная территория)
При окклюзии ствола задней мозговой артерии развивается инфаркт с одно- или двусторонним вовлечением субталамуса и медиального таламуса, а также поражением на одноименной стороне ножки мозга и среднего мозга с соответствующими клиническими симптомами. Очевидно, при нефункционирующем состоянии задней соединительной артерии (например, её атрезии являются также симптомы поражения периферической территории, кровоснабжаемой посткоммунальным сегментом задней мозговой артерии). Если полная окклюзия возникает не в начале задней мозговой артерии, то гемиплегия при инфаркте ножки мозга развивается редко. Синдромы частичного проксимального поражения позволяют думать об окклюзии среднемозговой таламо-перфоративной артерии, но не служит её подтверждением.
При синдроме верхнего поражения, характеризующемся вовлечением красного ядра и/или денто-рубро-таламического пути, отмечают грубую контралатеральную атаксию.
При синдроме нижнего поражения наблюдают паралич III черепного нерва и контралатеральную атаксию (синдром Клода) или паралич III черепного нерва в сочетании с контралатеральной гемиплегией (синдром Вебера).
При вовлечении в процесс субталамического льюисова тела возможно появление контралатерального гемибаллизма.
Окклюзия артерии Percheron вызывает парез взора вверх и гиперсомнию. Такому поражению часто сопутствуют абулия и состояние эйфории, способствующее возникновению абулии.
и МРТ головного мозга позволяют обнаружить двусторонние очаги поражения, напоминающие по своим очертаниям бабочку, в субталамусе и средненижних отделах таламуса. Обширные очаги инфаркта в среднем мозге и субталамусе при двусторонней окклюзии ствола задней мозговой артерии обычно развиваются вторично при эмболиях. В таких случаях наблюдают глубокую кому, двустороннюю пирамидную симптоматику и «децеребрационную ригидность».
Атероматозная окклюзия пенетрирующих ветвей таламических и таламо-геникулятной группы в их начальных участках приводит к появлению таламических и таламо-капсулярных лакунарных синдромов. Наиболее известен таламический синдром Дежерина-Русси. Основными его проявлениями служат контралатеральное выпадение как поверхностной (болевой и температурной), так н глубокой (тактильной и проприоцептивной) чувствительности по гемитипу. Иногда страдают лишь болевая и температурная либо вибрационная и мышечно-суставная чувствительность. Чаще всего нарушения определяются в области лица, руки, кисти, туловища, ноги н стопы, реже — лишь в одной конечности. Нередко имеет место гиперпатия, а спустя несколько недель или месяцев в поражённых областях может развиться мучительная жгучая боль. Больные описывают её как сдавливающую, стягивающую, леденящую, режущую. Эта боль носит упорный, изнурительный характер, слабо поддаётся воздействию анальгетиков. Иногда эффективны антиконвульсанты.
При вовлечении в очаг поражения заднего бедра внутренней капсулы обнаруживаются гемипарез или гемиплегия в сочетании с расстройствами чувствительности по гемитипу. К числу других сопутствующих двигательных нарушений относятся гемибаллизм, хореоатетоз, интенционный тремор, дискоординация и позная установка кисти и руки, особенно во время ходьбы.
Посткоммунальные синдромы (периферическая или кортикальная территория)
Инфаркты в области подушки зрительного бугра могут возникать при закупорке задней таламической таламо-геникулятной пенетрирующей ветви посткоммунального отдела задней мозговой артерии. Сама по себе окклюзия периферического отдела задней мозговой артерии чаще всего приводит к развитию инфарктов кортикальной поверхности медиальной стороны височной и затылочной долей. Частым симптомом бывает контралатеральная гомонимная гемианопсия. Бели ассоциативные зрительные поля остаются интактными и в патологический процесс вовлекается лишь кора вблизи шпорной борозды, больной ощущает дефект зрения внезапно. Иногда выпадает лишь верхний квадрант поля зрения. Центральное зрение может оставаться сохранным, если кровоснабжение вершины затылочного полюса поддерживается из ветвей средней мозговой артерии.
При вовлечении медиальных отделов височной доли и гиппокампа могут появляться внезапные расстройства памяти, особенно при поражении доминантного полушария, но эти нарушения, как правило, исчезают, поскольку функции памяти осуществляются обоими полушариями мозга.
При поражении доминантного полушария с распространением инфаркта в латеральном направлении глубоко в белое вещество с вовлечением в патологический процесс валика мозолистого тела возможно развитие алексии без аграфии. Также могут наблюдаться зрительная агнозия на лица, предметы, математические символы и цвета, а также аносмия с парафазиями (амнестическая афазия), даже в отсутствие поражения мозолистого тела.
При окклюзии внутренней сонной артерии резкий стеноз или окклюзия задней мозговой артерии на той же стороне способны уменьшить кровоток в зоне смежного кровоснабжения задней и средней мозговых артерий. Часто это приводит к возникновению зрительной агнозии, зрительного игнорирования и неспособности пересчитать предметы, находящиеся в противоположной половине поля зрения. Иногда окклюзия задней мозговой артерии сопровождается педункулярным галлюцинозом (зрительные галлюцинации в виде ярко расцвеченных сцен н предметов), но точная локализация инфаркта в таких случаях остаётся не до конца ясной.
Двусторонние инфаркты в бассейне кровоснабжения дистального отдела задней мозговой артерии приводят к развитию корковой слепоты. Больной часто не отдаёт себе отчёта в имеющихся расстройствах зрения, а зрачок нормально реагирует на свет. Даже когда зрительный дефект бывает полностью одно- или двусторонним, могут сохраняться небольшие островки зрения; при этом больной обычно сообщает о неустойчивости зрения, впечатлении, будто образы объектов ему удаётся удерживать за счёт сохранности видения их отдельных частей. В редких случаях утрачивается только периферическое зрение, а центральное остаётся интактным; при этом пациент сообщает о наличии трубчатого зрения.
Оптическая атаксия (неспособность осуществлять зрительный контроль за движениями конечностей), окулярная атаксия (неспособность переводить взгляд на определённую точку поля зрения), неспособность к счёту объектов, изображённых на картинке, или составлению представления об изображении на картине, неспособность обходить встречающиеся на пути предметы характерны для двусторонних поражений ассоциативных зрительных путей. Подобное сочетание симптомов носит название синдрома Балинта. Обычно он наблюдается при двусторонних инфарктах, развивающихся, как полагают, на фоне снижения кровотока в бассейне дистального отдела задней мозговой артерии в зоне смежного кровоснабжения со средней мозговой артерией, что бывает при остановке сердца.
Наконец, окклюзия верхней части основной артерии, обусловленная, как правило, эмболией, может давать клиническую картину, включающую все или любой из симптомов поражения центральной или периферической территории кровоснабжения. Патогномоничными для неё являются внезапное начало заболевания и двусторонний характер симптоматики.
Варианты развития артерий головного мозга и эпилепсия
Сложившиеся представления о механизмах развития церебральной ишемии подразумевают возникновение несоответствия между имеющимся кровоснабжением и потребностями мозговой ткани. К наиболее важным достижениям в области клинической ангионеврологии относится современная концепция гетерогенности ишемического инсульта, в основе которой лежит представление о многообразии причин и механизмов развития острого очагового ишемического повреждения мозга. Величина обратимого и необратимого повреждения мозга в значительной степени зависит от состояния гемодинамического, коллатерального, перфузионного и метаболического резервов мозга. Патологическая извитость магистральных артерий головы — наследственно детерминированная функциональная неполноценность соединительной ткани — встречается не менее чем у 10 % населения. Среди основньгх форм поражений интракраниальных артерий выделяют перегибы и петлеобразования, аневризматические расширения артерий, артериовенозные аневризмы. Чрезмерная извилистость сосудов способствует формированию в них тромбов. У 71 % больных с окклюзией артерий отмечен извитой ход сосудов. Недоразвитие артерий головного мозга в виде гипоплазии или стеноза задней нижней мозжечковой артерии и/или базилярной артерии, редко нижняя передняя мозжечковая артерия и извитость позвоночной артерии являются причинами снижения слуха и глухоты. Слабые анастомозы артерий головного мозга вызывают церебральную ишемию после дискэктомии шейного отдела позвоночника. При болезнях Паркинсона и Альцгеймера нейровизуализационные и патологоанатомические исследования в 20-30 % случаев обнаружили цереброваскулярные поражения, а в основе деменции может быть сосудистое заболевание головного мозга. Структурные изменения сосудов головного мозга, снижение скорости кровотока и наличие в 30 % стеноза в средней мозговой артерии могут стать предпосылками развития инсульта у больных с синдромом апноэ во сне.
При аномалии Киммерле необходимо учитывать наличие врожденных изменений позвоночных артерий. Диспластические нарушения в области краниовертебрального перехода в 2 раза чаще отмечены при патологической извитости позвоночных артерий, в меньшей степени за счет гипоплазии позвоночных артерий. До 51,9 % больных с мальформацией Киари и сирингомиелией имеют особенности строения артериального круга большого мозга. Извитости, асимметрии и гипоплазии позвоночных артерий с признаками нарушения кровотока характерны для вертебробазилярной недостаточности вследствие шейной дорсопатии и отмечены в 76,6 % случаев при центральном вестибулокохлеарном синдроме.
Артериальное русло головного мозга оказывается пораженным и при таких системных заболеваниях организма, как ревматоидный артрит, узелковый полиартериит, болезнь Такаясу, болезнь Шенлейна-Геноха, При проведении стоматологических манипуляций у больных с болезнью Штурге-Вебера или Реклингхаузена как типичных нейрофиброматозов возможно развитие угрожающего кровотечения. Первичное поражение церебральных артерий в виде васкулита и эндартериита лежит в основе развития нейросифилиса и приводит к вторичному страданию нервной ткани и возникновению инфарктов в головном мозге. Церебральный васкулит и герпетический церебральный васкулит могут развиться на фоне герпетической инфекции. При ишемических инсультах в 70 % наблюдений в ткани головного мозга, наряду с изменениями, обусловленными острым нарушением мозгового кровообращения, отмечаются очаговые поражения, сходные с изменениями при менингоэнцефалитах, вызванных опоясывающим и простым герпесом.
Изменения строения артерий головного мозга необходимо учитывать при оценке онкологических метастазов, а также у 40 % больных с тяжелой черепно-мозговой травмой при выявлении травматических субарахноидальных кровоизлияний и сопутствующего ангиографического вазоспазма.
По ходу выполнения изысканий по изучению взаимосвязи вариантов артерий головного мозга человека с цереброваскулярными расстройствами в рамках острых нарушений мозгового кровообращения и хронической ишемии головного мозга у нас сложились наблюдения о взаимосвязи вариантов строения и топографии артерий головного мозга человека с рядом других нозологических единиц. В этой связи мы представляем результаты собственных исследований о вариантах развития артерий головного мозга человека с различными видами эпилепсий.
Нами было проанализировано состояние артериального русла головного мозга 748 амбулаторных и стационарных пациентов от 22 лет до 81 года, находившихся на обследовании и лечении в неврологических и нейрохирургическом отделениях ОКБ № 2 им. профессора И.Н. Аламдарова г. Астрахани в период 1983-1998 гг., неврологических отделениях Городской больнтщы № 3 и Городской больницы № 4 г. Тамбова, нейрохирургическом отделении Тамбовской областной больницы, реабилитационно-оздоровительном комплексе семьи «Б. Липовица», неврологических кабинетах и в дневных стационарах Городской больницы № 4, Узловой поликлинике на ст. Тамбов ОАО «РЖД» и ЦДЛ ООО «Тамбовмедсервис», а также в амбулатории «Домашний доктор» (г. Тамбов) в течении 1998-2009 гг.
Всем пациентам проводилось комплексное клинико-инструментальное исследование, включающее данные клинического обследования невролога, терапевта и офтальмолога, стандартные лабораторные данные, электрокардиографию, флюорографию или обзорную рентгенографию органов грудной клетки. По показаниям были проведены консультации и обследования у нейрохирурга, гинеколога, отоларинголога, кардиолога, эндокринолога и психотерапевта; исследование когнитивной сферы по краткой шкале оценки психического статуса или миниисследование психического статуса, транскраниальная допплерография, электроэнцефалография. Всем пациентам были вьшолнены магнитно—резонансная томография (МРТ) и магнитно-резонансная ангиография (МРА).
Согласно полученным данным, варианты строения и топографии артериального круга большого мозга верифицированы всего в 27 случаях (61,4 % наблюдений) из 44 больных с эпилепсией или энцефалопатиями с ведущими эпилептиформными синдромами. Среди проанализированной группы пациентов с различными видами эпилепсий выявлены следующие варианты строения и топографтии артериального круга большого мозга: 1) изгиб обеих передних мозговых артерий у 1 (3,7 %) пациента; 2) гипоплазия левой позвоночной артерии у 2 (7,4 %) пациентов; 3) задняя трифуркация обеих внутренних сонных артерий и передняя трифуркация левой внутренней сонной артерии, гипоплазия базилярной артерии у 3 (11,1 %) пациентов; 4) передняя трифуркация левой внутренней сонной артерии, гипоплазия базилярной артерии у 6 (22,2 %) пациентов (рис. 1); 5) гипоплазия правой позвоночной артерии, аплазия задней соединительной артерии справа у 4 (14,8 %) пациентов; 6) гипоплазия правой позвоночной артерии, гипоплазия базилярной артерии у 5 (18,5 %) пациентов (рис. 2); 7) передняя трифуркация левой внутренней сонной артерии, гипоплазия задней соединительной артерии` гипоплазия правой задней мозговой артерии у 3 (11,1 %) пациентов;  извитость обеих позвоночных артерий у 2 (7,4 %) пациентов; 9) гипоплазия и извитость обеих позвоночных артерий у 1 (3,7 %) пациента, Ниже приведены достаточно показательные клинические наблюдения из совокупности собственных исследований.
извитость обеих позвоночных артерий у 2 (7,4 %) пациентов; 9) гипоплазия и извитость обеих позвоночных артерий у 1 (3,7 %) пациента, Ниже приведены достаточно показательные клинические наблюдения из совокупности собственных исследований.
Пример 1. Пациентка Н., 54 лет, наблюдается в Узловой поликлинике на ст. Тамбов ОАО «РЖД» с диагнозом: энцефалопатия как неуточненная (эпилептическая и дисциркуляторная) с полиморфными пароксизмами (по типу паралича Тодда) на фоне аномалий строения артерий головного мозга. Жалобы на шум в голове, шаткость при ходьбе, приступы слабости в правых конечностях и потери сознания. Неврологически: в сознании менингознаков нет, когнитивные функции снижены, эмоционально лабильна, зрачки d = s, конвергенция ослаблена, легкая слабость мимических мышц справа, парез правой кисти до 4 баллов, чувствительных нарушений нет, сухожильные рефлексы повышены d > s, в позе Ромберга пошатывание, координаторные пробы выполняет с промахиванием DetS, тремор век. Окулист: гипертонический ангиосклероз сосудов сетчаток обоих глаз. Терапевт: гипертоническая болезнь II степени, степень тяжести артериальной гипертонии II, категория риска 3. БАК: холестерин — 4,5 ммоль/л, β-липопротеиды — 3,5 г/л, креатинин — 69 мкмоль/л, мочевина — 7,9 ммоль/л. Протромбин — 88 %, фибриноген — 4.25 г/л. ЭКГ: син, ритм 80 в мин., нормальное положение ЭОС. МРТ и МРА: отображены на рисунке 1. Амбулаторное лечение: пирацетам, глицин, кавинтон, циннаризин, аминалон, энап, престариум, индопамин. Прошла курс лечения в дневном стационаре: мексидол, магния сульфат, престариум, индопамид, милдронат, эналаприл. Жалобы сохранились прежние. Неврологически — в сознании менингознаков нет, когнитивные функции снижены, черепные нервы без динамики парез правой кисти до 4,5 баллов, в пробе Ромберга пошатывание, координаторные пробы с интенцией с обеих сторон. Консультирована в Тамбовской психиатрической больнице, где поставлен диагноз: последствия органического поражения ЦНС сложного генеза с полиморфными пароксизмами. ЭЭГ: выраженные общемозговые изменения биори биоэлектрической активности, α-активности практически нет. По всем регионам полири менее 5 мкв. Регионарность, реакция активации отсутствуют, усвоения нет. Стойкая дезорганизация деятельности срединных структур. Заинтересованность левой височной области, где выявлен очаг медленноволнового раздражения. Низкое функциональное состояние коры с высокой чувствительностью ее к гипоксии, со снижением порога возбудимости ствола. Одиночные разряды заднестволовых отделов. Сосудистые влияния выражены. Катамнез: на фоне приема депакина-хроно жалобы значительно уменьшились, приступов не отмечено.
Пример 2. Пациент ВН., 21 год, наблюдается в Узловой поликлинике на ст. Тамбов ОАО «РЖД» с диагнозом: эпилепсия с полиморфными церебральными пароксизмами и когнитивными нарушениями. Наблюдается с детства — жалобы на приступы с потерей сознания. После начала лечения с 14 лет в неврологическом отделении Тамбовской областной детской больницы состоял на учете с диагнозом: эпилепсия, парциальные приступы с вторичной генерализацией. ЭЭГ (Психиатрия и наркология, 17.04.02): пароксизмальной активности не выявлено, Неустойчивый α-ритм. Дисфункция диэнцефальной области. Сосудистые влияния с повышенной вегетативной возбудимостью (15.06.04): ОМИ умеренные, но стойкие, с низкоамплитудной дизритмией. Регионарность нечеткая. Реакция активации снижена, усвоения нет. Грубой медленноволновой или пароксизмальной активности не выявлено. Снижена реактивность коры. Высокая вегетативная возбудимость. Сосудистые влияния 22.02.05: по сравнению с 15.06.04, положительная динамика. Общемозговые изменения умеренные, регуляторного характера. Умеренная дисфункция диэнцефальной области с усилением ее активности. Появился неустойчивый α-ритм, фрагментарный. Улучшилась реактивность коры. Несколько повысилась чувствительность коры к РФС, что приводит к снижению порога возбудимости заднестволовых структур. Пароксизмальных тенденций коры нет. Повышена вегетативная возбудимость. МРТ и МРА: отображены на рисунке 2. Неврологически: в сознании менингознаков нет, когнитивные функции несколько снижены, эмоционально лабилен, дистальный гипергидроз, тремор век и вытянутых пальцев рук, зрачки d = s, конвергирует, слабость мимических мышц справа, в позе Ромберга легкое пошатывание, координаторные пробы выполняет, парезов, чувствительных нарушений нет, сухожильные рефлексы d = s, симптом Бабинского слабоположителен с обеих сторон, Эпилептолог: когнитивные расстройства вследствие эпилепсии. Постоянно получает финлепсин (приступы связывает с нерегулярным приемом препарата).
Таким образом, считаем необходимым, сделать следующие выводы. 1. Варианты строения и топографии артериального круга большого мозга могут рассматриваться в качестве предикторов эпилептиформных феноменов структур головного мозга. 2. При различных церебральных пароксизмах, очевидно, есть целесообразность в исследовании артериального круга большого мозга. 3. Варианты строения и топографии артериального круга большого мозга в каждом конкретном случае следует рассматривать с точки зрения малых аномалий развития.
Диагностика и лабораторное обследование при ишемическом инсульте в бассейне задней мозговой артерии
Инфаркт в периферической территории бассейна задней мозговой артерии можно легко диагностировать с помощью магнитно-резонансной томографии (МРТ) и компьютерной томографии (). Между тем данные недостаточно надёжны при инфарктах в центральной зоне кровоснабжения задней мозговой артерии, особенно развивающихся вторично при окклюзирующем поражении пенетрирующих ветвей задней мозговой артерии. При магнитно-резонансной томографии (МРТ) головного мозга можно обнаружить инфаркты данной локализации диаметром более 0,5 см.
Ангиография остаётся единственным методом, убедительно демонстрирующим атеросклеротические изменения или эмболическое поражение задней мозговой артерии. Последняя из разновидностей современной спиральной компьютерной ангиографии (СКТ ангиография) с внутривенным контрастированием позволяет выявить окклюзирующее поражение мелких пенетрирующих ветвей задней мозговой артерии.
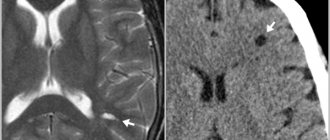
МРТ головного мозга пациента с внутримозговым кровоизлиянием в таламус (указаны стрелками).
Таким образом диагностика при ишемическом инсульте в бассейне задней мозговые артерии основывается главным образом на клинических данных, подтверждаемых результатами магнитно-резонансной томографии (МРТ) и компьютерной ангиографии (СКТ ангиографии) с внутривенным контрастированием.
Синдром недостаточности кровотока в артериях вертебробазилярной системы
Максимова М.Ю., Пирадов М.А. РМЖ. 2021. №7. С. 4-8 Статья посвящена проблеме синдрома недостаточности кровотока в артериях вертебробазилярной системы. Представлены методы диагностики и лечения вертебробазилярной недостаточности, которое должно быть направлено на предупреждение ее прогрессирования, улучшение кровоснабжения мозга, коррекцию отдельных синдромов и симптомов.
Самостоятельное клиническое понятие «синдром недостаточности кровотока в артериях вертебробазилярной системы» сформировалось в 1950-х гг., в период пересмотра взглядов на патогенез ишемических нарушений мозгового кровообращения (НМК) и становления концепции о ведущей роли при этом сосудистой мозговой недостаточности [1]. Особенности строения и функций этой артериальной системы, обеспечивающей питание жизненно важных структур мозга, и своеобразие клинической симптоматики при нарушениях кровотока в ней обусловили выделение ее в последней версии международной классификации в самостоятельный симптомокомплекс — «синдром вертебробазилярной артериальной системы» в рамках «преходящих транзиторных церебральных ишемических приступов (атак) и родственных синдромов» (Международная классификация болезней 10-го пересмотра, G45.0). Еще раньше группой экспертов Всемирной организации здравоохранения «вертебробазилярная недостаточность» определялась как «обратимое нарушение функции мозга, вызванное уменьшением кровоснабжения области, питаемой позвоночными и базилярной артериями». Подчеркивались ишемическая природа и обратимый характер нарушений, однако не указывалась длительность неврологической симптоматики, что ранее не позволяло отнести их к транзиторным ишемическим атакам (ТИА) и что стало возможным в настоящее время. Нарушения кровотока в артериях вертебробазилярной системы составляют около 70% всех ТИА. Инсульт с локализацией очаговых изменений в областях мозга, получающих кровь по артериям этой системы, развивается в 2,5 раза реже, чем в регионах, относящихся к бассейнам артерий каротидной системы [1].
Причины синдрома недостаточности кровотока в артериях вертебробазилярной системы
К основным причинам синдрома недостаточности кровотока в артериях вертебробазилярной системы, обусловленного артериальной гипертензией (АГ) и атеросклерозом (АС), относятся [1, 2]:
- атеростеноз или атерооблитерация одной из позвоночных артерий;
- характерная для АГ извитость артерий, которая в ряде случаев может привести к перегибу позвоночной артерии с формированием септального стеноза и нарушению кровотока в ней;
- врожденные аномалии позвоночных артерий (гипоплазия одной из позвоночных артерий, латеральное смещение устья позвоночной артерии), при которых недостаточность кровотока по одной из позвоночных артерий компенсируется другой позвоночной артерией, однако на фоне АС и АГ наступает декомпенсация;
- сдавление позвоночной артерии остеофитом в костном канале шейного отдела позвоночника, суставным отростком при нестабильности шейного отдела позвоночника, добавочным шейным ребром, спазмированной мышцей шеи (задняя лестничная мышца, длинная мышца шеи, нижняя косая мышца головы), что чаще всего наблюдается при врожденном аномально высоком вхождении позвоночной артерии в позвоночный канал — на уровне 3–5 шейных позвонков.
Cиндром недостаточности кровотока в артериях вертебробазилярной системы может также наблюдаться:
- при подключичном «синдроме обкрадывания», при котором в результате окклюзии подключичной артерии поступление крови не только во всю вертебробазилярную систему, но и в руку осуществляется лишь по одной позвоночной артерии;
- при окклюзии или выраженном атеростенозе обеих внутренних сонных артерий
(ВСА), т. к. в кровоснабжении полушарий большого мозга значительную роль играет вертебробазилярная система и при определенных условиях может возникнуть «синдром обкрадывания»; - при нарушениях общей гемодинамики.
Для подключичного «синдрома обкрадывания» характерен феномен, когда у больного во время интенсивной работы руки (кровоснабжаемой ретроградно из контралатеральной позвоночной артерии) возникают стволовые симптомы — чаще всего головокружение. Определенный вклад в развитие синдрома недостаточности кровотока в вертебробазилярной системе могут вносить изменения реологических свойств крови (повышение уровня фибриногена, вязкости крови, агрегации тромбоцитов и гематокрита, увеличение ригидности эритроцитов), приводящие к ухудшению микроциркуляции.
Диагностика недостаточности кровотока в артериях вертебробазилярной системы
Субъективные данные
Диагноз недостаточности кровотока в артериях вертебробазилярной системы основывается на характерном симптомокомплексе, объединяющем несколько групп клинических симптомов, встречающихся у больных АС и АГ. Это зрительные и глазодвигательные расстройства, нарушения статики и координации движений, вестибулярные нарушения. При этом предположительный диагноз определяется на основе не менее двух из указанных симптомов. Они кратковременны и нередко проходят сами по себе, хотя являются признаком нарушений кровотока в артериях этой системы, что требует клинического и инструментального обследования. Особенно необходим тщательный анамнез для уточнения обстоятельств возникновения тех или иных симптомов [1, 2].
Зрительные нарушения
включают в себя ощущение неясности видения, фотопсии, скотомы, изменения полей зрения, снижение остроты зрения и связаны с преходящей ишемией затылочных долей мозга. Неясность видения в форме пелены перед глазами и затуманивания зрения нередко возникает на высоте головной боли. Фотопсии проявляются в виде вспышек цветных точек, чаще всего красных или зеленых, черных, со светлым ореолом, а также пятен, огненных молний, линий, колец, зигзагов. От радужных кругов, характерных для глаукомы, фотопсии отличаются тем, что их появление не связано с внешним источником света; они возникают и при закрытых глазах. Изменение полей зрения наблюдается обычно в форме их концентрического сужения. Снижение остроты зрения часто развивается после появления головной боли и прогрессирует; зрение заметно ухудшается в период приступов головной боли и после них.
Глазодвигательные нарушения
проявляются в виде преходящей диплопии с негрубыми парезами мышц глаза и нарушенной конвергенцией. У большинства больных эти нарушения относятся к начальным проявлениям заболевания, а у четверти из них служат одной из главных жалоб при вертебробазилярной недостаточности. Статическая и динамическая атаксия относится также к числу постоянных симптомов, которые проявляются жалобами больных на неустойчивость и пошатывание при ходьбе и стоянии. Координация движений нарушена значительно меньше, стойкое изменение ее встречается, как правило, при инфарктах мозжечка.
Вестибулярные нарушения
проявляются в виде внезапного головокружения — системного, для которого характерно ощущение «вращения предметов», «перевернутой комнаты», и несистемного с ощущением «укачивания», тошнотой, реже рвотой. Обнаруживается также спонтанный нистагм, иногда только после специальных проб с поворотами головы в сторону и фиксацией ее в этих позах (проба Де Клейна). Развитие головокружения связывают с ишемией или преддверно-улиткового органа, или вестибулярных ядер и их связей. Вестибулярные ядра наиболее чувствительны к ишемии и гипоксии. При этом головокружение как моносимптом может расцениваться в качестве признака нарушения кровотока в артериях вертебробазилярной системы только в сочетании с другими признаками его нарушения у больных с относительно стойким отоневрологическим симптомокомплексом. Менее известны, хотя встречаются нередко, оптико-вестибулярные расстройства. К ним относятся симптомы «колеблющейся тени» и «конвергентного головокружения», при которых больные испытывают головокружение или неустойчивость при мелькании света и тени или при взоре, направленном вниз. Характерными симптомами являются приступы
внезапного падения
без потери сознания («дроп-атаки»), возникающие обычно при резких поворотах или запрокидывании головы. Описан синкопальный вертебральный синдром Унтерхарншайдта, при котором наблюдаются утрата сознания и гипотония мышц при отсутствии данных за эпилепсию и другие пароксизмальные состояния. К проявлениям
диэнцефальных
расстройств относятся резкая общая слабость, непреодолимая сонливость, нарушения ритма сна и бодрствования, а также различные вегетативно-висцеральные нарушения, внезапное повышение артериального давления (АД), нарушения сердечного ритма. Эти нарушения связаны с ишемией структур ретикулярной формации ствола мозга. Описанный симптомокомплекс дополнен в настоящее время другими признаками, которые в сочетании с ними также позволяют судить о недостаточности кровотока в артериях вертебробазилярной системы. На различных стадиях вертебробазилярной недостаточности больные нередко предъявляют жалобы на
снижение памяти
(«забывчивость»), расстройства концентрации и неустойчивость активного внимания. Чаще всего снижается память на имена, числа, недавно происшедшие события. Снижается способность к запоминанию нового материала, становится труднее удерживать в памяти прочитанное, забывается то, что намечено к осуществлению, возникает необходимость записывать. Больным становится трудно осмыслить большое количество информации, что приводит у лиц, занятых умственным трудом, к определенному снижению работоспособности, ограничению творческих возможностей. В то же время профессиональная память и память на прошлые события сохраняются. Это больше относится к оперативной памяти, чем к логической. Нередко снижение памяти и работоспособности расценивается окружающими как результат переутомления, а не как проявление сосудистой мозговой недостаточности. При нейропсихологическом исследовании отмечаются сохранность уровня обобщения, соответствие суждений общеобразовательному и культурному уровню, сохранность запаса представлений и навыков. Нарушения когнитивных функций существенно снижают качество жизни, а также оказывают влияние на прогрессирование сосудистой мозговой недостаточности. Снижение памяти на текущие события у больных с вертебробазилярной недостаточностью связано с хронической ишемией медиальных частей височных долей, прежде всего гиппокампа и сосцевидных тел. При вертебробазилярной недостаточности отмечаются и приступы транзиторной глобальной ишемии, при которой на несколько часов нарушается оперативная память (способность к запоминанию новой информации). Больной выглядит рассеянным, он дезориентирован в пространстве и времени, иногда возбужден, настойчиво пытается выяснить у окружающих, где находится, как оказался здесь, но будучи не в состоянии запомнить ответы, постоянно задает одни и те же вопросы. С возвращением способности к запоминанию восстанавливается и ориентация, амнезируется лишь сам эпизод. Причиной острой амнезии может служить и острое НМК в бассейнах обеих задних мозговых артерий. В этом случае амнезии могут сопутствовать ограничение полей зрения (односторонняя или двусторонняя гемианопсия), зрительная агнозия, алексия, амнестическая афазия, нарушение чувствительности. Сочетание ряда характерных симптомов позволяет диагностировать синдром недостаточности кровотока в артериях вертебробазилярной системы, хотя при этом определяются лишь ишемический характер НМК и локализация очага ишемии, а не причины, обусловившие этот характер.
Объективные данные
Наиболее доступными и безопасными для определения недостаточности кровотока в артериях вертебробазилярной системы являются неврологический осмотр и ультразвуковые методы исследования сосудистой системы мозга. Среди объективных признаков, выявляемых при
неврологическом осмотре
, следует прежде всего назвать нистагм, статическую и динамическую атаксию. В пробе Ромберга больной отклоняется в сторону. Ходьба с закрытыми глазами выявляет у пациента с недостаточностью кровотока в вертебробазилярной системе шаткость и стойкое отклонение в одну из сторон. При проведении пробы Унтербергера пациента просят маршировать на одном месте с закрытыми глазами в течение 1–3 мин. В норме он остается на месте или незначительно смещается относительно исходной точки либо слегка поворачивается вокруг оси. Патологическими считаются смещение вперед более чем на 1 м и поворот более чем на 40–60° (после 50 шагов на месте). Подобным образом интерпретируют результаты пробы Бабинского — Вейля («звездная проба»). Пациента просят с закрытыми глазами сделать два шага вперед, развернуться на 180° и сделать два шага назад. Любые отклонения в сторону или ротация указывают на нарушение функции вестибулярного лабиринта. Если пациента просят пройти в прямом и обратном направлении несколько раз, то в результате отклонения в одну из сторон траектория его движения напоминает очертания звезды (отсюда название пробы). Необходимо также измерить АД на обеих руках в положении сидя и лежа. К объективным признакам синдрома относятся разница пульса и АД на руках и шум в надключичной области. При значительном снижении систолического АД (более 20 мм рт. ст.) в вертикальном положении симптоматику, напоминающую недостаточность кровотока в вертебробазилярной системе, следует отнести за счет ортостатической гипотензии. Для подключичного «синдрома обкрадывания» характерен феномен, когда у больного на фоне интенсивной работы рукой возникают стволовые симптомы — чаще головокружение.
Ультразвуковая допплерография
позволяет получать данные о кровотоке в позвоночных артериях, линейной скорости и направлении потоков крови в них. Компрессионно-функциональные пробы дают возможность оценить состояние и ресурсы коллатерального кровообращения, кровоток в сонных, височных, надблоковых и других артериях. Дуплексное сканирование позволяет определить состояние стенки артерий, строение и поверхность атеросклеротических бляшек, стенозирующих эти артерии. Транскраниальная допплерография с фармакологическими пробами имеет значение для определения церебрального гемодинамического резерва. Исключительно информативны данные о состоянии магистральных артерий головы (МАГ) и интрацеребральных артерий, получаемые при КТ и МРТ в режиме ангиографии. При
рентгенографии
шейной части позвоночника могут быть получены данные о состоянии структур вокруг позвоночных артерий и воздействии этих структур на позвоночные артерии и кровоток в них; при этом используются функциональные пробы. Особое место в ряду инструментальных методов занимает
отоневрологическое исследование
, особенно если оно подкрепляется электронистагмографическими и электрофизиологическими данными о слуховых вызванных потенциалах, характеризующих состояние структур ствола мозга, а также МPТ этих структур. Алгоритм применения перечисленных инструментальных методов исследования определяется логикой построения клинического диагноза.
Лечение вертебробазилярной недостаточности
Лечение вертебробазилярной недостаточности направлено на предупреждение ее прогрессирования, улучшение кровоснабжения мозга, коррекцию отдельных синдромов и симптомов. Наиболее эффективными мерами в этом направлении являются исключение или коррекция основных
факторов риска
развития вертебробазилярной недостаточности, к которым относятся курение, гиперлипидемия, АС артерий мозга, АГ, сахарный диабет, ожирение, заболевания сердца, нарушения реологических свойств крови, психоэмоциональное перенапряжение, злоупотребление алкоголем [3]. Большое место в профилактике прогрессирования вертебробазилярной недостаточности занимают оздоровительные мероприятия, климатолечение на местных курортах, в условиях мелкогорья, на морских курортах, бальнеолечение (радоновые, рапные, углекислые, сульфидные, йодобромные ванны). Нужны умеренные физические нагрузки (лечебная гимнастика, ходьба, плавание) и регулярные умственные нагрузки.
Диета
не должна быть тягостной для больного (не переедать, ограничить потребление животных жиров, легкоусвояемых углеводов и продуктов, богатых холестерином, уменьшить общую калорийность пищи, ввести в рацион свежие овощи и фрукты, изделия из муки грубого помола, рыбные продукты). Исключается курение и ограничивается потребление алкоголя. При лечении вертебробазилярной недостаточности следует провести следующие мероприятия: раннее ее выявление; определение выраженности клинической симптоматики; исключение или коррекция основных факторов риска развития сердечно-сосудистых заболеваний; динамическое наблюдение; своевременное начало лечения; его длительность и непрерывность; лечение сопутствующих соматических, неврологических и психических нарушений; медицинская, профессиональная и социальная реабилитация. К
методам медикаментозного лечения
хронических НМК относятся: гипотензивная терапия, применение гиполипидемических средств, улучшение кровоснабжения мозга с использованием антитромботических препаратов, нейропротекционная терапия [3, 4]. Одним из наиболее перспективных с позиции доказательной медицины нейропротекционных препаратов является
цитиколин
[4, 5]. Цитиколин — природное эндогенное соединение, известное также как цитидин-5’-дифосфохолин (ЦДФ-холин), представляет собой мононуклеотид, состоящий из рибозы, цитозина, пирофосфата и холина. При пероральном приеме цитиколин быстро абсорбируется и в стенке кишечника и печени гидролизуется на холин и цитидин. Эти вещества поступают в системный кровоток, проходят через гематоэнцефалический барьер и вновь соединяются, образуя в пределах центральной нервной системы цитиколин [6]. Фосфатидилхолин мембран клеток головного мозга под действием фосфолипаз в условиях ишемии распадается до жирных кислот и свободных радикалов. За счет восстановления активности Na+/K+-АТФ-азы клеточной мембраны, снижения активности фосфолипазы A2 и участия в синтезе фосфатидилхолина реализуется мембраностабилизирующий эффект цитиколина. Кроме того, цитиколин влияет на образование свободных жирных кислот, синтез ацетилхолина и увеличение содержания норадреналина и дофамина в нервной ткани. Цитиколин также способен ингибировать глутамат-индуцированный апоптоз и усиливать механизмы нейропластичности [7]. Первые исследования цитиколина, проведенные в конце ХХ в., касались пациентов с сосудистой деменцией. Так, R. Lozano et al. (1986) наблюдали 2067 пожилых пациентов, находившихся на лечении в отделениях гериатрической психиатрии, и выявили положительное влияние 2-месячного курса терапии цитиколином на выраженность нейропсихологических симптомов [8]. В исследовании B. Chandra (1992), посвященном оценке эффективности препарата у 146 пациентов с сосудистой деменцией, было продемонстрировано, что терапия цитиколином в дозе 750 мг/сут в/в в течение 2 мес. приводила к достоверному улучшению показателей когнитивных функций (оценке по шкале MMSE) по сравнению с плацебо. Более того, эффект от терапии сохранялся через 10 мес. после окончания курса лечения [9]. В 2005 г. был опубликован Кокрановский обзор эффективности цитиколина в терапии когнитивных и поведенческих нарушений, обусловленных хронической цереброваскулярной недостаточностью, у пожилых пациентов [10]. В обзор вошли результаты 14 рандомизированных плацебо-контролируемых исследований с участием 1336 пациентов. Средняя доза цитиколина в указанных исследованиях составила 1000 мг/сут, продолжительность лечения — 3 мес. Эффективность лечения оценивалась по тестам на показатели памяти, внимания, поведения. В обзоре продемонстрированы позитивное влияние цитиколина на поведенческие нарушения, а также улучшение памяти. Единственным существенным ограничением данного обзора являлась небольшая продолжительность включенных в него клинических исследований. В последующие годы исследователи сосредоточились на изучении эффективности препарата у пациентов с умеренными когнитивными расстройствами (УКР) и постинсультными когнитивными нарушениями. Так, по данным М. В. Путилиной (2009), уже на начальных этапах проявлений когнитивных нарушений у пациентов с хронической сосудисто-мозговой недостаточностью применение цитиколина (в дозировке 1000 мг в/м или в/в в течение 10 сут с последующим пероральным приемом в виде раствора для приема внутрь в течение 3 мес.) способствует регрессу данных нарушений. Кроме того, препарат положительно влияет на сопутствующие эмоционально-аффективные и поведенческие расстройства в этой группе больных [11]. В 2013 г. опубликованы результаты двух контролируемых исследований, оценивающих влияние препарата на когнитивные функции у пациентов с хроническими цереброваскулярными заболеваниями. В плацебо-контролируемом исследовании L. Alvarez-Sabin et al. (2013) приняли участие 347 пожилых пациентов (средний возраст — 67,2±11,3 года), перенесших инсульт и имевших когнитивные нарушения. В группе активного лечения (172 пациента) цитиколин назначался в дозе 2000 мг/сут per os в течение 6 мес., далее по 1000 мг/сут еще 6 мес. Критериями эффективности лечения являлись результаты нейропсихологического обследования (батарея тестов на память, внимание, исполнительные (регуляторные) функции, ориентацию во времени), а также оценка клинических исходов по модифицированной шкале Рэнкина через 6 и 12 мес. после начала лечения. На фоне длительной терапии цитиколином отмечались замедление прогрессирования когнитивных расстройств и лучшее функциональное восстановление (по сравнению с плацебо) за счет улучшения внимания, регуляторных функций и ориентации во времени [12]. Исследование IDEALE было посвящено оценке эффективности цитиколина в длительной терапии сосудистых УКР у пожилых пациентов. 349 пациентам с УКР преимущественно сосудистого генеза назначался цитиколин (265 больных) в дозе 1000 мг/сут per os в течение 9 мес. или плацебо (84 пациента). Терапия цитиколином не влияла на показатели функциональной повседневной деятельности по сравнению с плацебо. Вместе с тем на фоне лечения цитиколином отмечалась положительная динамика когнитивных функций при их оценке по шкале MMSE (улучшение через 9 мес. в среднем на 0,5 балла), в группе плацебо наблюдалось прогрессирование когнитивных нарушений (через 9 мес. — ухудшение в среднем на 1,9 балла) (р=0,0001). Таким образом, длительная терапия цитиколином сопряжена со снижением темпов прогрессирования когнитивных нарушений у пациентов с сосудистыми УКР [13]. В последнее время широко внедряются в практику новые воспроизведенные лекарственные формы. Среди них — отечественный препарат
Нейпилепт
. Препарат выпускается из японской субстанции компании KYOWA в виде раствора 125 и 250 мг/мл для в/в и в/м введения, а также двух пероральных форм — раствора для приема внутрь 100 мг/мл во флаконах по 30 мл и 100 мл. Объем флакона 100 мл соответствует форме выпуска оригинального препарата в саше. В рамках пострегистрационных многоцентровых рандомизированных исследований были проведены сравнение Нейпилепта с оригинальным препаратом у 152 пациентов в остром периоде ишемического инсульта в каротидной системе (РКИ № 396 от 24.06.2013) [14] и изучение эффективности и безопасности его пероральной формы у 128 пациентов с когнитивными нарушениями (РКИ № 145 от 26.03.2015) [15]. Результаты исследований продемонстрировали сопоставимые с оригинальным препаратом переносимость и эффективность Нейпилепта при указанных состояниях [16, 17].
Заключение
Следует подчеркнуть, что своевременно начатое и систематически проводимое лечение может предотвратить прогрессирование сосудисто-мозговой недостаточности и значительно улучшить качество жизни пациентов. Особое значение приобретают адекватность и эффективность приема цитиколина (Нейпилепта). Адекватность терапии подразумевает курсовой прием препарата, а также сотрудничество пациента и лечащего врача при назначении и проведении лечения, целями которого являются сохранение трудоспособности и поддержание качества жизни пациента. Могут быть рекомендованы следующие направления оценки эффективности лечения вертебробазилярной недостаточности (уже через 6–12 мес. от начала лечения): уменьшение или исчезновение церебральных жалоб, улучшение когнитивных функций (в первую очередь памяти).
Оригинальная статья опубликована на сайте РМЖ (Русский медицинский журнал): https://www.rmj.ru/articles/nevrologiya/Sindrom_nedostatochnosti_krovotoka_varteriyah_vertebrobazilyarnoy_sistemy/#ixzz5NyXkC9vV
Форма записи на приём…
Лечение ишемического инсульта в бассейне задней мозговой артерии
Инфаркты головного мозга в бассейне задней мозговой артерии обычно бывают вторичного характера и развиваются на фоне эмболии из нижележащих сегментов вертебрально-базилярной системы или из полости сердца. С целью предупреждения повторных эмболий просвета артерий назначают антикоагулянты (гепарин). При атеросклеротической окклюзии задней мозговой артерии специфического лечения не требуется. Симптомы транзиторной ишемической атаки головного мозга в бассейне задней мозговой артерии могут быть обусловлены атеротромботическим стенозом её проксимального (нижележащего) участка или одной из её пенетрирующих ветвей (лакунарная ТИА).
Течение такого атеросклеротического поражения задней мозговой артерии остаётся неуточнённым. Поэтому нет чётких сравнительных данных об эффективности антикоагулянтов и антиагрегантов либо назначения той или иной терапии в сравнении с отсутствием таковой. В целом же наиболее мягким способом лечения ишемии или ишемического инсульта в бассейне задней мозговые артерии представляется назначение антиагрегантов (аспирин, трентал).
Ишемический инсульт (инфаркт мозга) — симптомы и лечение
Общие мероприятия
При лечении ишемического инсульта принято не снижать артериальное давление быстро, если оно высокое, особенно в первые дни заболевания. Низкое артериальное давление следует повысить — этим занимаются врачи, не давайте самостоятельно пациенту никаких лекарств.
Несдерживаемая сильная рвота — частая проблема в периоде сразу после инсульта, особенно при поражении в бассейне основной артерии. Это создаёт проблемы в питании больного. Если рвота не прекращается, или есть дисфагия, то ставят зонд для питания. Нехватку электролитов восполняют инфузионной терапией. Следует внимательно отслеживать проходимость дыхательных путей.
Тромболитическая терапия
Тромболитическая терапия — это единственная терапия ишемического инсульта в остром периоде, эффективность которой доказана в крупных исследованиях.
С момента появления первых симптомов инсульта до введения тромболитика должно пройти не более 4,5 часов, поэтому важна быстрая госпитализация.
Окклюзия сосудов происходит в артериальном или венозном русле. Тромботические лекарства растворяют тромб, но препарат необходимо доставить в зону тромбоза.
Тромболитические средства впервые появились в 40-х годах XX века. Активная разработка лекарств этой группы привела к тому, что в настоящее время выделяют пять поколений тромболитиков:
- Первые тромболитики — это природные вещества, которые переводят плазмаген в плазмин, тем самым вызывают активное кровотечение. Выделяют эти ингредиенты из крови. Данную группу лекарств используют редко, так как возможно сильное кровотечение. К этому поколению относят: Фибринолизин, Стрептокиназа, Урокиназа, Стрептодеказа, Тромбофлюкс.
- Второе поколение — это вещества, полученные на основе достижений генной инженерии с помощью бактерий. Это поколение лекарств хорошо изучено, у них практически отсутствуют побочные эффекты. Действуют непосредственно на тромбы. К этому поколению относят: Алтеплаза, Актилизе, Проурокиназа, Гемаз. Пуролаза, Метализе.
- Третье поколение — эти препараты способны быстро находить тромб и более продолжительно на него воздействовать. Максимально эффективны в первые три часа: Ретеплаза, Тенектеплаза, Ланотеплаза, Антистреплаза, Антистрептолаза.
- Четвёртое поколение — эти препараты находятся в разработке, отличаются быстрым и интенсивным воздействием на тромб. Недостаточно изучены.
- Пятое поколение — это совмещение натуральных и рекомбинантных активных веществ.
В фазе восстановления, когда состояние больного практически всегда в той или иной степени улучшается, важное значение имеет логопедическая помощь, а также трудотерапия и ЛФК.
Инфузионная терапия
Антикоагулянты (гепарин и непрямые антикоагулянты) назначают только тогда, когда предписания врача заведомо будут выполняться, и есть возможность следить за свёртываемостью крови [8].
Антикоагулянты
Антикоагулянты препятствуют образованию нитей фибрина и тромбообразованию, способствуют прекращению роста уже образовавшихся тромбов, а также воздействию на тромбы эндогенных фибринолитических ферментов [11].
Лечение антикоагулянтами может быть начато только после исключения внутримозгового кровотечения.
Прямые коагулянты: гепарин и его производные, прямые ингибиторы тромбина, а также селективные ингибиторы фактора Х (Фактор Стюарта — Прауэра — одного из факторов свёртывания крови).
Непрямые антикоагулянты:
- Антагонисты витамина К: фениндион (фенилин), варфарин (варфарекс), аценокумарол (синкумар);
- Гепарин и его производные: гепарин, антитромбин III, далтепарин (фрагмин), эноксапарин (анфибра, гемапаксан, клексан, эниксум), надропарин (фраксипарин), парнапарин (флюксум), сулодексид (ангиофлюкс, вессел дуэ ф), бемипарин (цибор);
- Прямые ингибиторы тромбина: бивалирудин (ангиокс), дабигатрана этексилат (прадакса);
- Селективные ингибиторы фактора Х: апиксабан (эликвис), фондапаринукс (арикстра), ривароксабан (ксарелто).
Антиагреганты
Назначение антиагрегантов позволяет улучшить прохождение жидкости в тканях мозга и предотвратить развитие острого нарушения кровоснабжения головного мозга [6].
Антиагреганты не позволяют тромбоцитам склеиваться, тем самым препятствуют формированию тромбов.
Классификация антиагрегантов по механизму действия:
- аспирин, индобуфен, трифлюза (прекращают действие циклооксигеназы-1, ЦОГ-1);
- тиклопидин, клопидогрел, празугрел, тикагрелор, кангрелор (прекращают работу рецептора АДФ Р2Y12 на тромбоцитарных мембранах);
- абциксимаб, монофрам, эптифибатид, тирофибан; ксимелофибан, орбофибан, сибрафибан, лотрафибан и другие (антагонисты гликопротеинов (GP) Iib/IIIa);
- дипиридамол и трифлюзал (ингибиторы цАМФ фосфодиэстеразы);
- илопрост (усилитель аденилатциклазы);
- ифетробан, сулотробан и другие (подавляют рецептор ТХА2/PGH2);
- атопаксар, ворапаксар (противодействуют рецептору AR (protease activated receptors) тромбина).
Аспирин — часто используемый препарат из этой группы. Если антикоагулянты противопоказаны, то можно использовать антиагреганты.
Хирургическое лечение
Каротидная эндартерэктомия — это профилактическая хирургическая операция, которая проводится с целью удаления атеросклеротических бляшек из arteria carotis communis (общей сонной артерии).
При развитии мозжечкового инсульта со сдавлением ствола мозга с целью сохранить жизнь больного выполняют хирургическую операцию для снятия внутричерепного давления в задней черепной ямке.
Противоотёчная терапия
По поводу применения кортикостероидов при ишемическом инсульте существуют разные и достаточно противоположные мнения, но всё же они активно пользуются врачами для уменьшения отёка мозга: назначают дексаметазон 10 мг внутривенно струйно или внутримышечно, затем по 4 мг внутривенно или внутримышечно каждые 4-6 часов.
Осмотические средства.Маннитол — повышает осмолярность плазмы, тем самым жидкость из тканей, в том числе и из головного мозга, перемещается в кровяное русло, создаётся выраженный мочегонный эффект, и из организма выводится большое количество жидкости. Отмена может дать рикошетный эффект.
Противосудорожные средства
Их необходимо назначать при развитии ишемического инсульта с эпилептическими припадками.
Реабилитация после инсульта
Реабилитационные мероприятия начинают уже в раннем периоде заболевания и продолжают после выписки из стационара. Они включают в себя не только проведение медикаментозного лечения, массажа, лечебной физкультуры, логопедических занятий, но и требуют привлечения других специалистов по психологической, социальной и трудовой реабилитации.
Наряду с восстановлением нарушенных функций, реабилитация включает:
- профилактику постинсультных осложнений;
- профилактику повторных инсультов.
Основные принципы реабилитации после инсульта:
- раннее начало реабилитационных мероприятий;
- систематичность и длительность, что возможно при хорошо организованном поэтапном построении реабилитации;
- включение в реабилитационный процесс специалистов различных профилей, индивидуализация реабилитационных программ;
- активное участие в реабилитационном процессе самого больного, его близких и родных.
Длительность реабилитации определяется сроками восстановления нарушенных функций. Восстановление двигательных функций происходит в основном в первые 6 месяцев после инсульта. В этот период проведение интенсивной двигательной реабилитации наиболее эффективно. Восстановительное лечение больных с афазией должно быть более длительным и проводиться в течение первых 2-3 лет после инсульта.
Комплексность реабилитации состоит в использовании не одного, а нескольких методов, направленных на преодоление дефекта.
При двигательных нарушениях комплекс реабилитации включает:
- методы кинезотерапии (пассивную и активную гимнастику, обучение ходьбе и навыкам самообслуживания);
- коррекцию нарушения двигательной функции с помощью биологической обратной связи и электростимуляцию с помощью обратной связи;
- методы преодоления спастичности и лечение артропатий.
При речевых нарушениях основным являются регулярные занятия со специалистом по восстановлению речи, чтения и письма (логопедом-афазиологом или нейропсихологом).
Наиболее оптимальна следующая модель этапной реабилитации после инсульта:
1-й этап — реабилитация начинается в ангионеврологическом (или в обычном неврологическом отделении клинической больницы), куда больной доставляется машиной скорой помощи;
2-й этап — по окончании острого периода (первые 3-4 недели) возможны следующие варианты направления больных:
- 1-й вариант — больной с полным восстановлением нарушенных функций выписывается на амбулаторное долечивание или переводится в санаторий;
- 2-й вариант — больной с выраженным двигательным дефицитом, к концу острого периода ещё самостоятельно не передвигающийся или передвигающийся с большим трудом, нуждающийся в посторонней помощи при самообслуживании, переводится в реабилитационное отделение той больницы, куда он был доставлен машиной скорой помощи;
- 3-й вариант — больные с умеренным и лёгким двигательным дефектом, самостоятельно передвигающиеся в пределах больницы, элементарно обслуживающие себя, переводятся в реабилитационный центр. В реабилитационный центр переводятся также больные, которые за время пребывания в реабилитационном отделении больницы (2-й вариант) научились самостоятельно ходить и элементарно обслуживать себя в быту.
3-й этап — амбулаторная реабилитация: реабилитация в специальных реабилитационных санаториях и на дому.
Амбулаторную реабилитацию осуществляют на базе реабилитационных отделений поликлиник или восстановительных кабинетов или в форме «дневного стационара» при реабилитационных отделениях больниц и реабилитационных центрах. В реабилитационных санаториях могут находиться больные, полностью себя обслуживающие и самостоятельно передвигающиеся не только в помещении, но и вне его. Тем больным, которые не могут самостоятельно добраться до поликлиники или дневного стационара, реабилитационную помощь (занятия с методистом лечебной физкультуры и занятия по восстановлению речи) оказывают на дому, обязательно обучая родственников.
Противопоказания и ограничения к проведению активной реабилитации
Следующие сопутствующие заболевания ограничивают или препятствуют проведению активной двигательной реабилитации:
- частые приступы стенокардии;
- сердечная недостаточность;
- высокое и плохо снижаемое артериальное давление;
- хронические лёгочные заболевания: бронхиальная астма с частыми приступами, обструктивный бронхит;
- тяжёлые формы сахарного диабета;
- рак;
- острые воспалительные заболевания;
- некоторые болезни и патологии опорно-двигательного аппарата: тяжёлые артриты и артрозы, ампутированные конечности.
Психозы, выраженные когнитивные нарушения (деменция) являются ограничением для проведения не только двигательной, но и речевой реабилитации.
Существуют ограничения для восстановительного лечения в обычных реабилитационных центрах: крайне ограниченная подвижность больных (отсутствие самостоятельного передвижения и самообслуживания), нарушение контроля функций тазовых органов, нарушение глотания. Реабилитацию таким больным, а также пациентам с выраженными сердечной и лёгочной патологиями проводят в реабилитационных отделениях, расположенных на базе крупных клинических многопрофильных больниц, по специальным реабилитационным программам.