Александра Коростышевская, Андрей Савелов, Ирина Приходько, Яна Исаева, Василий Ярных «Наука из первых рук» № 3(88), 2020
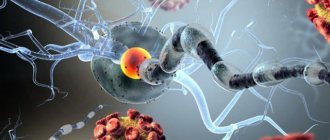
С детства мы слышим, что нервные клетки не восстанавливаются. И хотя вопрос о возможности образования новых нейронов во взрослом мозге до сих пор открыт, уже есть данные, что процесс нейрогенеза у человека продолжается до глубокой старости. Любые нарушения в развитии нервных клеток могут приводить к серьезным, иногда необратимым патологиям. Одним из таких нарушений являются дефекты в защитной изоляционной оболочке (миелине) отростков нервных клеток, которые могут формироваться у человека еще до его рождения. Их практически невозможно диагностировать с помощью традиционных методов визуализации.
Об авторах
| Александра Михайловна Коростышевская — доктор медицинских наук, ведущий научный сотрудник лаборатории МРТ-технологий, заведующая диагностическим отделением института «Международный томографический центр» Сибирского отделения РАН. Автор и соавтор более 70 научных работ. |
| Андрей Александрович Савелов — кандидат физико-математических наук, старший научный сотрудник лаборатории МРТ-технологий института «Международный томографический центр» Сибирского отделения РАН. Автор и соавтор более 90 научных работ. |
| Ирина Юрьевна Приходько — инженер-программист лаборатории МРТ-технологий института «Международный томографический центр» Сибирского отделения РАН. Автор и соавтор 3 научных работ. |
| Яна Олеговна Исаева — студентка Института медицины и психологии им. В. Зельмана Новосибирского государственного университета. |
| Василий Леонидович Ярных — кандидат химических наук, заведующий лабораторией отделения радиологии, профессор университета Вашингтона (Сиэтл, США) и Томского государственного университета. Автор и соавтор более 70 научных работ, в том числе 5 патентов. |
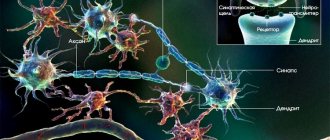
В мозге человека в среднем содержится около 100 млрд нейронов, которые принимают, хранят, обрабатывают и передают информацию с помощью электрических и химических сигналов. Взаимодействие между нейроном и другими нервными клетками и органами происходит с помощью коротких (дендриты
) и длинного (
аксон
) отростков.
Каждый аксон, подобно проводу, покрыт изоляционным материалом — миелиновой оболочкой
, которая обеспечивает более высокую скорость прохождения нервных импульсов и защищает нервные волокна от повреждений. Кроме того, эта оболочка несет опорную функцию, а также, по последним данным, служит для аксона, нуждающегося в большом количестве энергии, своего рода «заправочной станцией».
Аксон — главный «кабель» нейрона, покрытый миелиновой оболочкой. Он отдаленно напоминает линию электропередач с цепочкой изоляторов. Цель оболочки, которую формируют специальные обслуживающие клетки (олигодендроциты либо клетки Шванна), — обеспечить передачу электрических импульсов без потерь и с максимальной скоростью. © Servier Medical Art. Слева
— аксоны седалищных нервов мыши (
красные
), обернутые клетками Шванна (
зеленые
, ядра —
синие
). Фото A. Alvarez-Prats и T. Balla. © Eunice Kennedy Shriver /
National Institute of Child Health and Human Development
/ NIH
Все повреждения миелиновой оболочки или дефекты, возникшие в период ее формирования, приводят к серьезным, иногда неизлечимым заболеваниям. Среди них наиболее известен рассеянный склероз
— хроническое аутоиммунное заболевание, поражающее преимущественно молодых людей.
Разрушается миелин и при инсультах
, которые встречаются не только у взрослых (в первую очередь, как принято считать, у пожилых людей), но и у детей, включая нерожденных. Внутриутробный инсульт чаще всего случается после 28-й недели беременности, у детей — через месяц после рождения. Инсульт у плода приводит к развитию пороков головного мозга, а у детей может вызвать
детский церебральный паралич
в раннем возрасте.
При этом о «качестве» миелинизации головного мозга конкретного человека мы сегодня судим лишь по косвенным клиническим симптомам или данным магнитно-резонансной томографии
(МРТ), с помощью которой обычно удается обнаруживать дефекты миелина уже на поздней, часто необратимой стадии.
В головном мозге миелиновую оболочку создают олигодендроциты, в периферической нервной системе — клетки Шванна. Каждый олигодендроцит образует несколько «ножек», которые неоднократно «оборачиваются» вокруг части какого-нибудь аксона (внизу
). В результате один олигодендроцит оказывается связан с несколькими нейронами. © Servier Medical Art.
Вверху
— олигодедроциты в культуре (
красные
, ядра —
сиреневые
). © jakeyoung64
Не все знают, что миелин — это множество слоев клеточной мембраны, много раз «намотанных» на аксон. Формируется миелин плоскими выростами «служебных» глиальных клеток, цитоплазма в которых практически отсутствует. Миелиновая оболочка не непрерывна, а дискретна, с промежутками (перехватами Ранвье). Поэтому аксон обладает более быстрой скачкообразной проводимостью: скорость прохождения сигнала по волокнам с миелином и без него может отличаться в сотни раз. Что касается молекулярного состава «изолятора», то он, как и все клеточные мембраны, состоит преимущественно из липидов и белков.
Дефекты нервной «изоляции»
Развитие мозга плода — сложный процесс, при котором происходят быстрые перестройки морфологии и микроструктуры нервной ткани. В некоторых зонах мозга процесс формирования миелина начинается уже с 18–20-й недели беременности, а продолжается приблизительно до десятилетнего возраста.
Именно нарушения миелинизации часто лежат в основе задержек физического и умственного развития ребенка, а также служат причиной формирования ряда неврологических и психиатрических патологий. Помимо заболеваний, таких как инсульт, задержки развития головного мозга плода с нарушением миелинизации иногда наблюдаются и при многоплодной беременности. При этом десинхронизацию в развитии мозга близнецов оценить «на глаз» довольно сложно.
Но как выявить дефекты миелина в период внутриутробного развития? В настоящее время акушеры-гинекологи пользуются только биометрическими показателями (например, размером мозга), однако они обладают высокой изменчивостью и не дают полной картины. В педиатрии даже при наличии явных функциональных отклонений в мозговой деятельности ребенка традиционные изображения МРТ или нейросонографии
(ультразвукового исследования головного мозга новорожденных) часто не показывают структурные отклонения.
Поэтому поиск точных количественных критериев оценки формирования миелина во время беременности является актуальной задачей, которую к тому же нужно решить с помощью неинзвазивных диагностических методов, уже апробированных в акушерстве. Специалисты из новосибирского Международного томографического центра СО РАН предложили использовать для этих целей новый метод количественной нейровизуализации, уже адаптированный для дородовых (пренатальных
) исследований.
Новости о нейрорегенерации
«Нервные клетки не восстанавливаются», — говорили нам десятилетиями, но теперь даже школьники знают, что это неправда. Уже известно, что в мозге каждого взрослого человека есть как минимум одна область, где новые нервные клетки рождаются постоянно: это область гиппокампа. Она отвечает за обработку воспоминаний и за ориентацию в пространстве. Кстати, именно поэтому у таксистов передняя часть гиппокампа становится более развитой.
А в последние несколько месяцев появилось несколько научных работ, результаты которых показывают, что организм может самостоятельно восстановить даже, казалось бы, безвозвратно утерянные нервные клетки и связи.
Восстановить миелин при рассеянном склерозе
Ученые из Университета Калифорнии в Сан-Франциско успешно провели ряд экспериментов по восстановлению утраченного миелина у мышей с рассеянным склерозом.
В основе такого заболевания, как рассеянный склероз, лежит «атака» оболочек нейронов собственными иммунными клетками. Из-за этого утрачивается способность нейронов передавать нервные импульсы. Миелиновый слой, который покрывает длинные отростки нейронов, в данном случае выступает в роли «проводов», по которым «бежит» нервный импульс. Его разрушение замедляет прохождение импульса в 5–10 раз и приводит к слепоте, нарушениям чувствительности, параличам, когнитивным расстройствам и прочим неврологическим проблемам.
Специалисты использовали модель рассеянного склероза у мышей. При этом здоровым мышам делали инъекцию белка, содержащегося в миелиновой оболочке, инициируя таким образом аутоиммунный ответ организма, т. е. заставляя иммунитет «ополчиться» на собственные же ткани.
Читайте также: Нейронаука
Новый эксперимент опирался на предыдущее исследование, в котором эта же группа ученых обнаружила положительный эффект блокатора гистамина под названием клемастин. Исследователи применили клемастин совместно с белком, вызывающим рассеянный склероз у мышей, и показали, что у таких животных проявлялось значительно меньше симптомов заболевания, потому что происходило восстановление миелиновой оболочки аксонов нейронов спинного и головного мозга.
Восстановить зрительный нерв
Сложность поражений зрительного аппарата неизбежно влечет за собой и сложность восстановления функции. Особенно трудно приходится, когда заболевание или травма поражает нейроны, соединяющие сетчатку со зрительными нервами, или сами зрительные нервы.
Исследование, недавно опубликованное в Nature Neuroscience, открывает новые горизонты в восстановлении зрительных нервов. Коллектив ученых из Университета штата Юта, Гарвардского, Стэнфордского университетов и Калифорнийского университета в Сан-Диего получили интересные результаты эксперимента. Они травмировали зрительные нервы мышей пережатием. Контрольная группа не получала никакой терапии, вследствие чего спустя три недели у этих мышей отмечалась гибель клеток сетчатки. Другой группе демонстрировали сменяющиеся черно-белые изображения, стимулирующие сетчатку, что вызвало незначительную регенерацию нерва.
Ученые отметили также, что инъекция в глаз вирусного вектора, несущего ген, который отвечает за продукцию белка сRheb1 (стимулирует так называемый сигнальный путь мишени рапамицина у млекопитающих (mTOR), регулирующий клеточный рост), повышала эффективность восстановления.
Тщательный анализ показал, что комбинация этих методов ведет к регенерации аксонов ганглионарных клеток сетчатки, причем, что наиболее примечательно, эта регенерация оказалась очень специфичной. Аксоны прорастали к правильным зрительным целям, как бы возвращаясь на привычные места, не возникало нарушения функции, как это часто бывает при восстановлении нерва.
Это исследование явно демонстрирует, насколько велик резерв восстановления нервной ткани, даже у взрослых людей.
И просто нервные клетки
Конечно, самая страшная вещь, которая может случиться с мозгом, — это инсульт. Оксидативный стресс, вызванный или кровоизлиянием в мозг, или, наоборот, ишемией, недостатком кровоснабжения, приводит к массированной и быстрой гибели нейронов. К сожалению, нервные клетки после инсульта в коре головного мозга пока никому восстановить не удалось.
Однако стало возможным «распушить» связи у уцелевших нейронов. Недавние эксперименты, проведенные в Медицинской школе Университета Калифорнии в Лос-Анджелесе, показали, как сделать так, чтобы нервные клетки поскорее восстановились после инсульта.
Это стало возможным благодаря фактору роста и дифференциации 10 — GDF10 (growth and differentiation factor 10). Его введение в нервные ткани способствует росту нервных связей, в результате чего мозг быстрее «приходит в себя» после инсульта. Здоровые нейроны распространяют новые ростки («спруты») вглубь ткани и снова налаживают потерянные контакты.
Итак, мы видим, что ученые в содружестве с медиками постепенно нащупывают различные пути, благодаря которым можно «подстегнуть» восстановление самих нервных клеток, или получить новые нейроны взамен погибших, или заставить нервную ткань саму восстановить ущерб. А нам осталось только дождаться, пока эти исследования перейдут из лабораторных опытов в клинические испытания.
Алексей Паевский
Фото istockphoto.com
На обычном томографе
Любая патология головного мозга плода, которую подозревают врачи во время ультразвукового обследования беременной, обычно является показанием к проведению МРТ; подобные исследования проводятся в МТЦ СО РАН уже более десяти лет. Результаты МРТ могут подтвердить, уточнить, опровергнуть либо вообще изменить предварительный диагноз и, соответственно, тактику ведения беременности.
Дело в том, что количество миелина и размеры отдельных структур головного мозга у эмбриона настолько малы, что любые измерения очень сложны и трудоемки. К тому же плод постоянно шевелится, что очень затрудняет получение качественных изображений и достоверных количественных данных. Поэтому нужна технология, позволяющая получать изображения быстро и с высокой разрешающей способностью даже на маленьких объектах.
Именно таким оказался метод быстрого картирования макромолекулярной протонной фракции
(МПФ) — биофизического параметра, который описывает долю протонов в макромолекулах тканей, вовлеченных в формирование МРТ-сигнала, тогда как обычно источником сигнала являются протоны, содержащиеся в воде (Yarnykh, 2012; Yarnykh et al., 2015).
Метод макромолекулярной протонной фракции (МПФ) основан на эффекте переноса намагниченности, когда протоны свободной воды «обмениваются» намагниченностью с протонами малоподвижных макромолекул, таких как белки. Скорость этого процесса влияет на величину детектируемого сигнала МРТ и зависит от площади взаимодействия макромолекулярной фракции и воды
В основе метода лежит специализированная процедура математической обработки МРТ-изображений, которая позволяет вычленить компоненты сигнала, связанные с МПФ клеточных мембран. А в головном мозге человека и животных основная их часть содержится именно в миелине. Реконструируются карты МПФ на основе исходных данных, которые могут быть получены практически на любом клиническом томографе.
Для реконструкции карт МПФ используются четыре исходных изображения, полученные различными традиционными методами МРТ. Правильность такого подхода подтвердили результаты его апробации на лабораторных животных в Томском государственном университете: у мышей, которым вводили раствор, вызывающий разрушение миелина, результаты МПФ-картирования совпали с данными гистологического исследования тканей (Khodanovich et al., 2017).
Анатомия миелина в строении нерва
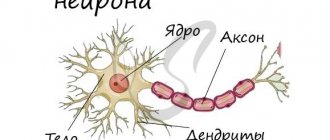
Главная клетка нервной системы – нейрон. Тело нейрона называется сома. Внутри нее находится ядро. Тело нейрона окружено короткими отростками, которые называются дендриты. Они отвечают за связь с другими нейронами. От сомы отходит один длинный отросток – аксон. Он несет импульс от нейрона к другим клеткам. Чаще всего на конце он соединяется с дендритами других нервных клеток.
Всю поверхность аксона покрывает миелиновая оболочка, которая представляет собой отросток клетки Шванна, лишенный цитоплазмы. По сути, это несколько слоев клеточной мембраны, обернутые вокруг аксона.
Шванновские клетки, обволакивающие аксон, разделяются перехватами Ранвье, в которых отсутствует миелин.
Роль микроглии в разрушении миелиновой структуры
Микроглия представляет собой макрофаги, способные к фагоцитозу и умеющие распознавать различные патогенные частицы – антигены. Благодаря мембранным рецепторам эти глиальные клетки вырабатывают ферменты – протеазы, а также цитокины, например, интерлейкин 1. Он является медиатором воспалительного процесса и иммунитета.
Миелиновая оболочка, функции которой заключаются в изолировании осевого цилиндра и улучшении проведения нервного импульса, может повреждаться интерлейкином. В результате этого, нерв «оголяется» и скорость проведения возбуждения резко снижается.
Более того, цитокины, активируя рецепторы, провоцируют избыточный транспорт ионов кальция в тело нейрона. Протеазы и фосфолипазы начинают расщеплять органеллы и отростки нервных клеток, что приводит к апоптозу – гибели данной структуры.
Она разрушается, распадаясь на частицы, которые и пожирают макрофаги. Это явление называется эксайтотоксичностью. Оно вызывает дегенерацию нейронов и их окончаний, приводя к таким заболеваниям, как болезнь Альцгеймера и болезнь Паркинсона.
Принципы лечения дефектов оболочки
Заболевания, связанные с разрушением мякотной оболочки, очень сложно лечить. Терапия направлена в основном на купирование симптомов и остановку процессов разрушения. Чем раньше диагностировано заболевание, тем больше шансов остановить его течение.
Возможности восстановления миелина
Благодаря своевременному лечению можно запустить процесс восстановления миелина. Однако, новая миелиновая оболочка не будет так же хорошо выполнять свои функции. Кроме того, болезнь может перейти в хроническую стадию, а симптомы сохранятся, лишь слегка сгладятся. Но даже незначительная ремиелинизация способна остановить ход болезни и частично вернуть утраченные функции.
Современные лекарственные средства, направленные на регенерацию миелина более эффективны, но отличаются очень высокой стоимостью.
Терапия
Для лечения заболеваний, вызванных разрушением миелиновой оболочки, используются следующие препараты и процедуры:
- бета-интерфероны (останавливают течение заболевания, снижают риск возникновения рецидивов и инвалидности);
- иммуномодуляторы (воздействуют на активность иммунной системы);
- миорелаксанты (способствуют восстановлению двигательных функций);
- ноотропы (восстанавливают проводниковую активность);
- противовоспалительные (снимают воспалительный процесс, вызвавший разрушение миелина);
- нейропротекторы (предупреждают повреждение нейронов мозга);
- обезболивающие и противосудорожные препараты;
- витамины и антидепрессанты;
- фильтрация ликвора (процедура, направленная на очищение спинномозговой жидкости).
Функции
Основными функциями миелиновой оболочки являются:
- изоляция аксона;
- ускорение проведения импульса;
- экономия энергии за счет сохранения ионных потоков;
- опора нервного волокна;
- питание аксона.
Как работают импульсы
Нервные клетки изолированы благодаря своей оболочке, но все же взаимосвязаны между собой. Участки, в которых клетки соприкасаются, называются синапсы. Это место, где встречаются аксон одной клетки и сома или дендрит другой.
Электрический импульс может передаваться внутри одной клетки или от нейрона к нейрону. Это сложный электрохимический процесс, который основан на перемещении ионов через оболочку нервной клетки.
В спокойном состоянии внутрь нейрона попадают только ионы калия, а ионы натрия остаются снаружи. В момент возбуждения они начинаются меняться местами. Аксон положительно заряжается изнутри. Затем натрий перестает поступать через мембрану, а отток калия не прекращается.
Изменение напряжения из-за движения ионов калия и натрия называется «потенциал действия». Он распространяется медленно, но миелиновая оболочка, обволакивающая аксон, ускоряет это процесс, препятствуя оттоку и притоку ионов калия и натрия из тела аксона.
Проходя через перехват Ранвье, импульс перескакивает с одного участка аксона на другой, что и позволяет ему двигаться быстрее.
После того, как потенциал действия пересекает разрыв в миелине, импульс останавливается, и возвращается состояние покоя.
Такой способ передачи энергии характерен для ЦНС. Что касается вегетативной нервной системы, в ней часто встречаются аксоны, покрытые малым количеством миелина или вообще не покрытые им. Скачки между шванновскими клетками не осуществляются, и импульс проходит гораздо медленнее.
Доставка лецитина
Лецитин, также известный как phophatidylcholine, представляет собой жирное вещество, состоящее из холина, жирных кислот и других липидных молекул. Лецитин важен для передачи нерва и может служить источником холина для производства миелина. Диетические источники лецитина включают яичные желтки, соевые бобы, зародыши пшеницы и печень. Брюссельская капуста, креветка, арахисовое масло и шоколад также содержат значительные уровни лецитина. Если вы следуете вегетарианской диете, которая исключает молочные продукты или яйца, вы рискуете стать дефицитными в лецитине и холине. Принимая вегетарианскую добавку лецитина, можно обеспечить достаточное потребление этих важных питательных веществ.