Паркинсонизм — это комплексный синдром, который проявляется характерными симптомами: нарушением походки, повышением мышечного тонуса, замедленностью движений и сложностями в удержании равновесия. Этот синдром классифицируют по причине возникновения, а одной из его разновидностей является сосудистый паркинсонизм. Основным этиологическим фактором являются заболевания церебральных сосудов, что приводит к органическому поражению центральной нервной системы (головного мозга). Болезнь склонна к прогрессированию, а патологические изменения часто необратимы. После проведения диагностики и подтверждения сосудистого компонента пациенту назначается поддерживающая терапия, направленная на стабилизацию состояния и предотвращение осложнений.
Определение
Паркинсонизм — это группа поражений нервной системы, которые проявляются рядом характерных симптомов. Однако по причине возникновения эти заболевания принято делить на несколько групп. К ним относятся:
- идиопатический паркинсонизм (болезнь Паркинсона) — возникает без определенной причины;
- вторичный (в том числе сосудистый, токсический, травматический и другие) — развивается на фоне патологий других систем органов;
- паркинсонизм, который возникает на фоне патологий центральной нервной системы.
Сосудистый паркинсонизм относится ко второй группе. Он является следствием органического поражения сосудов, которые участвуют в кровоснабжении головного мозга. Теория этого заболевания была подтверждена с развитием методик нейровизуализации. Заболевание довольно редкое, частота его возникновения составляет не более 2—15% всех случаев паркинсонизма. Чаще всего патология развивается после перенесенного ишемического инсульта либо вследствие дисциркулярной энцефалопатии. Среди пациентов — люди любого пола и возраста, чаще старше 40 лет.
Симптомы паркинсонизма
Паркинсонизм — второе по распространенности после болезни Альцгеймера нейродегенеративное заболевание. В основном оно характерно для пожилых людей, однако выделяют и ювенильную форму паркинсонизма, которая возникает до 20 лет. Болезнь чаще поражает мужчин, чем женщин.
Основными проявлениями паркинсонизма являются:
- тремор в руках или ногах, дрожание головы, нижней челюсти и т.д.
- несогласованность движения рук и ног во время ходьбы
- нарушение способности удерживать равновесие
- ригидность мышц позвоночника, конечностей, шеи, затрудненность, скованность и замедленность произвольных движений
- походка мелкими убыстряющимися шагами
- фиксация тела в так называемой позе просителя (туловище наклонено вперед, голова опущена к груди, руки и кисти в согнутом положении)
- бедность мимики, редкие мигания
- затруднения при выполнении сложных манипуляций
Кроме двигательных нарушений отмечают вегетативные расстройства (например, сальность лица, повышенное потоотделение, слюнотечение) и изменения психики (эмоциональная притупленность, аспонтанность).
По мере развития паркинсонизма тонус мышц повышается настолько, что пациент теряет способность обслуживать себя, основное время пребывает в положении лежа или сидя.
Причины и механизм развития
Синдром сосудистого паркинсонизма — это следствие нарушения работы экстрапирамидной системы. Она представляет собой скопление ганглиев (нервных узлов), черную субстанцию и других структур среднего мозга, которые регулируют двигательную активность и координацию движений. При нарушении кровоснабжения определенных отделов возникает характерный комплекс симптомов, который проявляется двигательными расстройствами. За кровообращение в тканях головного мозга отвечают церебральные сосуды разного диаметра. Причиной сосудистого паркинсонизма являются их патологии, вследствие чего отделы центральной нервной системы испытывают дефицит кислорода и питательных веществ.
Болезнь может проявляться в том числе при поражении сосудов мелкого калибра.
Причинами такого расстройства могут становиться следующие заболевания:
- гипертоническая энцефалопатия — нарушение работы отделов головного мозга, вызванное постоянным повышением артериального давления;
- склероз мелких артериол — разрастания плотной соединительной ткани вместо эластичной оболочки;
- амилоидоз сосудов — патология белкового обмена, которая протекает с отложением специфического белка (амилоида) в тканях;
- системная красная волчанка — хроническое аутоиммунное заболевание;
- антифосфолипидный синдром — аутоиммунная патология, связанная с образованием антител к фосфолипидам, которые являются одним из основных структурных компонентов клеточных мембран.
Поражение крупных церебральных артерий встречается редко. У таких пациентов диагностируют инсульты базальных ганглиев, что проявляется выраженной симптоматикой. Заболевания, которые могут приводить к таким последствиям:
- тромбоз средней мозговой артерии либо ее ветвей;
- атеросклероз сосудов головного мозга — появление плотных склеротических бляшек;
- артериовенозные мальформации — патология, при которой отсутствует капиллярная сеть, а кровь из артерий попадает непосредственно в вены;
- узелковый васкулит — воспаление стенок сосудов, в том числе может протекать с некротическим компонентом.
СПРАВКА! Сосудистый паркинсонизм регистрируется у 11% пациентов, которые перенесли инсульт головного мозга. Также его диагностируют в 14% случаев дисциркулярной энцефалопатии.
Основным патогенетическим звеном в развитии паркинсонизма является повышение артериального давления, в некоторых случаях — органические повреждения сосудистых стенок, снижение их прочности и эластичности. У таких пациентов повышается порозность стенок, вследствие чего жидкость беспрепятственно проникает за пределы артерий и накапливается в окружающих тканях. Это становится причиной отечности головного мозга, нарушения питания и кровоснабжения нервных клеток, а затем — их некроза (гибели). Регенеративные процессы протекают медленно, поэтому наблюдается развитие спонгиоза — губчатости белого вещества.
Основная причина нарушения работы головного мозга — это дефицит кровоснабжения его определенных отделов
Двигательная активность контролируется медиаторами — биологически активными веществами. Наиболее важными из них являются дофамины: они активируют движения мышц, оказывают возбуждающий эффект и устраняют скованность. При нарушении кровоснабжения клеток экстрапирамидной системы наблюдается гибель дофаминовых рецепторов. Равновесие нарушается, и регуляция двигательной активности осуществляется антагонистами дофамина — ацетилхолином и гамма-аминомасляной кислотой. Эти вещества производят обратный эффект, поэтому под их действием проявляются типичные признаки паркинсонизма.
Причины паркинсонизма
При паркинсонизме происходят изменения в структурах мозга: в частности, дегенерация клеток черной субстанции мозга. Именно эта структура отвечает за тонус мышц, регулирует моторную функцию, с ее участием происходят процессы дыхания, сердечная деятельность, поддерживается тонус сосудов.
Спровоцировать эти изменения могут многие факторы: инфекционные заболевания, атеросклероз, отравления различными веществами, в том числе угарным газом, свинцом, ртутью. Определенную роль играет и наследственный фактор, однако в этом случае паркинсонизм начинается раньше, в том числе и в юношеском возрасте.
Классификация
Сосудистый паркинсонизм может отличаться своими клиническими проявлениями. В зависимости от его причины, могут преобладать неврологические симптомы либо признаки нарушения кровообращения. Первая классификация выделяет три типа синдрома, исходя из характера его течения:
- острый — клиническая картина проявляется внезапно, но в дальнейшем не прогрессирует, возможно даже улучшение состояния больного;
- ступенеобразно прогрессирующий — периоды обострения чередуются с периодическими фазами ремиссии, во время которых наблюдается уменьшение выраженности симптомов;
- неуклонно прогрессирующий (наиболее редкий) — в течении болезни периоды улучшения отсутствуют, состояние пациента постоянно ухудшается.
Вторая классификация основана на этиологии синдрома паркинсонизма. Она выделяет два основных типа патологии, которые отличаются в том числе своими клиническими проявлениями.
- Постинсультная форма — развивается в течение первых 6—12 месяцев после перенесенного инсульта и связана с нарушением кровообращения в крупных сосудах. Течение чаще всего острое, при диагностике обнаруживаются одиночные участки ишемии. Проявления могут быть односторонними.
- Безинсультная форма возникает при поражении мелких церебральных сосудов. При визуализации отмечают диффузное повреждение мозговых структур, что является причиной двустороннего развития симптоматики. Болезнь чаще прогрессирует ступенеобразно.
СПРАВКА! Последний вариант развития сосудистого паркинсонизма (неуклонно прогрессирующий) наиболее опасен. Такой тип более характерен для органических патологий центральной нервной системы, поэтому при заболеваниях сосудистого генеза его диагностика затруднительна.
Паркинсонизм и его основные нозологические формы
Болезнь Паркинсона (БП) – хроническое, неуклонно прогрессирующее заболевание центральной нервной системы с дегенерацией нигростриарных нейронов и нарушением функции базальных ганглиев. Она относится к одним из наиболее частых нейродегенеративных заболеваний, которые стоят на третьем месте среди причин смертности после сердечно-сосудистых и онкологических заболеваний.
Паркинсонизм известен давно, первые сообщения о лечении похожих расстройств были сделаны 1000-2500 лет до н.э.
Первое клиническое описание принадлежит английскому врачу Джеймсу Паркинсону, который опубликовал в 1817 году «Эссе о дрожательном параличе».
Подробный клинический анализ комплекса патологии был сделан в 1879 г. знаменитым французским неврологом Жаном Мартеном Шарко.
В настоящее время в классификации паркинсонизма выделяют: I. Болезнь Паркинсона (она составляет около 70-80% всех регистрируемых случаев). II. Вторичный (симптоматический) паркинсонизм (около 15%) включает следующие варианты: лекарственный, токсический, постгипоксический, энцефалитический, травматический, при объемных процессах, при гидроцефалии, сосудистый. III. Паркинсонизм при различных дегенеративных заболеваниях с поражением экстрапирамидной системы («паркинсонизм-плюс», около 10%): мультисистемные атрофии (стриатонигральная дегенерация, оливопонтоцеребеллярная дегенерация), прогрессирующий надъядерный паралич (болезнь Стила-Ричардсона-Ольшевского), кортикобазальная дегенерация, деменция с тельцами Леви, паркинсонизм-БАС-деменция, болезнь Вильсона-Коновалова, болезнь Гентингтона (ювенильный вариант Вестфаля), болезнь Фара (идиопатическая кальцификация базальных ганглиев), болезнь Альцгеймера, другие.
Основной нозологической формой паркинсонизма является болезнь Паркинсона.
Распространенность БП во всем мире составляет приблизительно 1% .
Этиология БП неизвестна. В основе ее патогенеза лежит дегенерация так называемых дофаминергических нейронов. БП носит преимущественно спорадический характер, однако при наличии БП у ближайших родственников риск ее развития возрастает.
Клинические проявления БП возникают при уменьшении количества дофамина в хвостатом ядре и скорлупе не менее чем на 70%. Симптомы БП развиваются постепенно, вовлекая сперва конечности на одной стороне. Для клинической картины БП характерно сочетание гипокинезии, ригидности, тремора покоя, и постуральных нарушений.
Гипокинезия проявляется снижением двигательной активности, замедленностью движений, уменьшением амплитуды действий.
Тремор покоя в классических случаях начинается с дистальных отделов верхней или нижней конечности и напоминает движения рук «при счете монет или скатывании пилюль». В дальнейшем в тремор вовлекается гомолатеральная конечность, нижняя челюсть, противоположные конечности. Иногда отмечается постуральное дрожание рук.
Ригидность при БП проявляется пластическим повышением мышечного тонуса, часто — с феноменом «зубчатого колеса», нарастающим в процессе исследования. Постуральная неустойчивость, возникающая на развернутых стадиях БП, характеризуется неустойчивостью при поворотах, пошатыванием при ходьбе, падениями. В дальнейшем больные вынуждены использовать опорные приспособления.
Кроме двигательных нарушений, при БП части развиваются недвигательные проявления: нервно-психические расстройства; нарушения сна; вегетативные нарушения; чувствительные нарушения.
В зависимости от преобладания того или иного симптома в клинической картине БП принято выделять следующие клинические формы заболевания: дрожательную, акинетическую, а также смешанные формы — акинетико-ригидную и ригидно-дрожательную.
Выделяют пять степеней тяжести БП (стадии болезни по Хен и Яру): 1-я стадия — односторонние симптомы паркинсонизма; 2-я стадия — двусторонние симптомы паркинсонизма без постуральных нарушений; 3-я стадия — присоединяется умеренная постуральная неустойчивость; 4-я стадия — значительное ограничение двигательной активности, падения, но при этом еще сохраняется возможность самостоятельно передвигаться; 5-я стадия — больной прикован к постели или инвалидному креслу.
На поздних стадиях БП клиническая картина видоизменяется, появляются дополнительные моторные (двигательные флуктуации, лекарственные дискинезии, нарушения ходьбы, падения, застывания и акинетические кризы) и немоторные (вегетативные, когнитивные, нейропсихические) синдромы.
У больных могут возникать длительные периоды декомпенсаций — от нескольких дней до нескольких недель, а также акинетические кризы — тяжелые эпизоды акинезии, сопровождающиеся дисфагией, вегетативными нарушениями, гипертермией, олигурией, спутанностью сознания. Причинами этого могут являться: нарушение схемы приема противопаркинсонических средств, их полная о); прием препаратов, блокирующих ДА-рецепторы (прежде всего нейролептики); обострение сопутствующих соматических заболеваний, стресс; операции, травмы, дегидратация организма.
Диагностировать БП с уверенностью можно только с помощью аутопсии. Клиническая диагностика синдрома паркинсонизма требует обязательного наличия гипокинезии и не менее одного из трех основных симптомов паркинсонизма: тремора покоя, ригидности и постуральной неустойчивости.
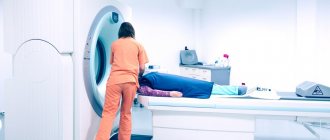
Проведение МРТ головного мозга является обязательным при наличии у больного синдрома паркинсонизма. Данное исследование прежде всего необходимо для дифференцирования идиопатической болезни Паркинсона и вторичного паркинсонизма, а также «паркинсонизма-плюс».
Основными направлениями лечения БП являются: 1. Фармакотерапия. 2. Медико-социальная реабилитация. 3. Лечебная физическая культура (ЛФК). 4. Нейрохирургическое лечение.
Фармакотерапия при БП направлена на нормализацию биохимического дисбаланса и требует постоянного приема лекарственных средств, так как при прекращении лечения симптомы БП возвращаются к исходному уровню.
На ранней стадии лечение БП заключается в назначении монотерапии с последующим переходом на комбинированное лечение.
На ранних стадиях заболевания общепринятым является назначение больным в возрасте до 70 лет агонистов ДА-рецепторов и ингибиторов МАО-В в виде монотерапии или сочетания.
У пациентов старше 70 лет, когда ожидаемая продолжительность жизни больного меньше, а также имеются когнитивные нарушения, терапию можно сразу начинать с ДОФА-содержащих препаратов в минимальной эффективной дозе, которую подбирают постепенно.
Холинолитики (Циклодол, Акинетон) назначаются преимущественно на ранней стадии БП — в виде монотерапии или в комбинации с другими противопаркинсоническими средствами; они преимущественно влияют на тремор покоя.
В настоящее время их назначают лишь молодым пациентам, с выраженным тремором покоя и сохранными когнитивными функциями. Высокая частота побочных эффектов и низкая эффективность по сравнению с другими группами существенно ограничивают их применение. Препараты амантадина (Мидантан, ПК-Мерц).
Амантадины могут назначаться как при начальной стадии в виде монотерапии, так и в комбинации с другими противопаркинсоническими средствами на поздних стадиях БП. Препараты эффективны и для уменьшении степени выраженности дискинезий, вызванных приемом леводопы. Инфузионная форма амантадина сульфата (ПК-Мерц) применяется при лечении декомпенсаций и акинетических кризов при БП.
Агонисты дофаминовых рецепторов обладают способностью непосредственно стимулировать ДА рецепторы в головном мозге. Неэрголиновые агонисты ДА-рецепторов (Проноран, Мирапекс, Реквип Модутаб, Ньюпро) широко применяются на всех стадиях БП. Помимо контроля двигательных нарушений, у них выявлен антидепрессивный эффект, что очень важно, так как частота депрессивного синдрома при БП достаточно высока.
Монотерапия АДАР на ранних стадиях заболевания позволяет отсрочить назначение препаратов леводопы, а также развитие моторных флюктуаций и лекарственных дискинезий.
Ингибиторы МАО типа В (Разагилин). Назначение препаратов этой группы приводит к увеличению количества дофамина в нейронах. Также предполагается наличие у них нейропротекторного действия. Могут назначаться на ранних стадиях в виде монотерапии, а также в комбинации с леводопой.
Ингибиторы КОМТ. Ингибиторы КОМТ увеличивают биодоступность леводопы, уменьшая уровень ее неактивных метаболитов.
Ингибиторы КОМТ периферического действия не проходят ГЭБ и препятствуют метилированию леводопы в желудочно-кишечном тракте и кровеносном русле. Благодаря этому они сохраняют концентрацию леводопы на определенном уровне. К таким препаратам относится энтакапон.
Комбинация энтакапона с препаратами леводопы позволяет снизить суточную дозу ДОФА-содержащего препарата на 15–30%.
Он назначается только в комбинации с препаратами леводопы (Сталево), так как при назначении в виде монотерапии самостоятельным противопаркинсоническим эффектом не обладает.
Препараты леводопы (Мадопар, Наком, Тремонорм, Тидомет-форте, Дуэллин, Синдопа). Дофамин не проходит ГЭБ, поэтому в качестве лекарственного препарата был предложен метаболический предшественник дофамина — леводопа, которая проходит через ГЭБ и в головном мозге метаболизируется в дофамин. На сегодняшний день препараты леводопы являются наиболее эффективными лекарственными средствами, «золотым стандартом», применяющимися для лечения БП. Однако они не останавливают прогрессирование БП. Более того, в среднем после 5 лет применения ДОФА-содержащих средств у больных БП снижается их эффект, появляются двигательные флюктуации и лекарственные дискинезии.
Сроки назначения терапии препаратами леводопы зависят от степени выраженности и темпа прогрессирования заболевания, профессиональной деятельности больного, семейно-бытового статуса. В целом назначать препараты этой группы необходимо, когда имеются выраженные двигательные нарушения, которые не удается купировать другими противопаркинсоническими средствами.
Нейрохирургическое лечение.
Снижение эффективности фармакотерапии, появление моторных флюктуаций и лекарственных дискинезий являются показанием к применению нейрохирургического лечения, которое в течение последних двух десятилетий прочно заняло свое место в алгоритме ведения пациентов с БП. В настоящее время используются три типа нейрохирургических вмешательств при БП: стереотаксические деструктивные методы (вентролатеральная таламотомия, паллидотомия, субталамотомия и их комбинация), стимуляционные методы (имплантация электродов в подкорковые структуры с последующей их хронической электростимуляцией) и внутримозговая трансплантация дофаминергических нейронов мезенцефалона эмбриона человека, эффективность которой продолжает изучаться.
Наиболее современный метод хирургического лечения БП – глубокая электростимуляция головного мозга. Процедура ГСМ состоит в имплантации электродов с 4 контактами в зоны-мишени в пределах подкорковых образований головного мозга; электроды соединяются с имплантируемым под кожу стимулятором, подающим высокочастотные электрические импульсы в стимулируемое ядро.
Медико-социальная реабилитация.
Высокая степень инвалидизации при неуклонно прогрессирующей БП, социально-экономические потери, которые несет общество обусловливают необходимость создания системы медико-социальной реабилитации, которая должна включать в себя диспансерное наблюдение больных; создание школ для пациентов и их родственников ведение обучающих программ и психотерапевтических занятий, создание общественных организаций, групп поддержки. Большое значение имеет ЛФК, которая может подбираться индивидуально в зависимости от степени тяжести болезни у конкретного больного, занятия ЛФК в группах, танцевальная терапия, а также трудотерапия, физиотерапия.
Литература: 1. Шток В. Н., Диагностика и лечение экстрапирамидных расстройств. — М., 2000. — С. 138. 2.Шток В. Н., Федорова Н. В. Лечение паркинсонизма. — М., 1997. — 194 с. 3.Яхно Н. Н. Современные подходы к лекарственному лечению болезни Паркинсона // Клиническая фармакология и терапия. — 1994. — № 3-4. — С. 92 — 97. 4.Левин О.С., Федорова Н.В., Болезнь Паркинсона.- М., — 2012. 5. Н.В. Федорова, И.П. Чигирь, Болезнь Паркинсона – Лечащий врач.- 2005г. -№8.- с.26-28.
Симптомы болезни
В большинстве случаев симптомы сосудистого паркинсонизма развиваются симметрично. Поскольку синдром проявляется на фоне острого нарушения кровообращения, клиническая картина включает признаки как сосудистой недостаточности, так и энцефалопатии. Выделяют несколько симптомокомплексов, которые прямо указывают на развитие паркинсонизма:
- нарушение походки — она становится замедленной, ноги пациента не отрываются высоко от пола, наблюдаются признаки ослабления мышц;
- ухудшение координации движений — при попытке сохранить центр тяжести корпус больного наклоняется вперед, а ноги сгибаются в коленях; в запущенных случаях могут возникать случаи падения во время ходьбы;
- снижение активности мелких мускулов, что приводит к отсутствию мимики, изменению почерка, сложностям при выполнении работы, связанной с мелкой моторикой;
- головные боли, головокружение, появление различных шумов в голове — эти признаки индивидуальны и проявляются не во всех случаях;
- регрессия интеллектуального развития, ухудшение памяти и внимания.
Клиническую картину вторичного паркинсонизма следует отличать от проявлений болезни Паркинсона. Для второго случая характерен мышечный тремор — дрожание мускулов конечностей, чаще кистей рук. При сосудистом паркинсонизме подобные признаки наблюдаются не более, чем у 4% больных, но присутствуют другие симптомы. Так, для этой болезни более характерно поражение нижних конечностей и хроническое ступенеобразное течение. Еще одним отличительным признаком будет реакция организма на лечение леводопой — при болезни Паркинсона этот препарат вызывает улучшение состояния.
Болезнь Паркинсона (паркинсонизм)
Определение.
Болезнь Паркинсона (БП) – хроническое заболевание головного мозга. Основные проявления (симптомы) заболевания связаны с уменьшением количества нервных клеток, вырабатывающих вещество дофамин. Дофамин участвует в передаче нервны импульсов для обеспечения нормальной двигательной активности. Недостаток дофамина в отделах мозга, участвующих в регуляции движений, является основной причиной замедленности и ограничения выполнения привычных движений.
Болезнь Паркинсона относится к первичному или идиопатическому паркинсонизму, который составляет 80-90 % от общего числа больных, имеющих синдром паркинсонизма. Вторичный паркинсонизм встречается значительно реже и составляет 10-15 %, например: сосудистый, лекарственный, токсический, постэнцефалитический, посттравматический, паркинсонизм при опухолях и гидроцефалии, на фоне метаболической энцефалопатии. Паркинсонизм в рамках нейродегенеративных заболеваний составляет 8-12 % (атипичный паркинсонизм, «паркинсонизм-плюс» — прогрессирующий надъядерный паралич, мультисистемная атрофия, болезнь диффузных телец Леви, кортикобазальная дегенерация).
Историческая справка.
Болезнь Паркинсона была описана около 200 лет назад (1817 год) английским врачом Джеймсом Паркинсоном в своем знаменитом «Эссе о дрожательном параличе», в котором обобщил результаты наблюдений за шестью пациентами. С тех пор БП была детально изучена, конкретизированы все её симптомы, однако портрет заболевания, составленный Дж. Паркинсоном, остается по-прежнему точным и ёмким.
Эпидемиология.
БП по распространенности занимает 4 место после деменции, эпилепсии, цереброваскулярной патологии у пациентов старшей возрастной группы. Таким образом, около 1-2% людей старше 65 лет страдают БП. В зависимости от того, в каком возрасте выявляются первые признаки БП, выделяют следующие формы: ювенильная форма – начало до 20 лет; раннее начало – до 40 лет; типичное начало – старше 60 лет.
Этиология.
Уже в течение многих лет обсуждается возможность генетической предрасположенности, но генетический фактор не всегда играет главную роль, т.к. на долю семейных форм паркинсонизма приходится всего около 5-10 %, в то время как спорадический паркинсонизм встречается в 80-90% случаев. Генетические факторы наибольшее значение играют при раннем начале заболевания, а в более поздней возрастной группе большее значение приобретают другие факторы, такие как инволюционные изменения в головном мозге и факторы внешней среды или токсические факторы.
Патогенез.
Патогенетическую основу БП составляет резкое уменьшение количества дофамина в черной субстанции и полосатом теле. Синтез дофамина происходит в телах дофаминергических нейронов, располагающихся в компактной зоне черной субстанции. Здесь он образуется в виде небольших пузырьков – гранул, которые по аксонам нигростиарных нейронов транспортируются к окончаниям аксонов в хвостатом ядре и скапливаются перед пресинаптической мембраной. Под влиянием приходящих нервных импульсов происходит выход квантов медиатора в синаптическую щель, который оказывает воздействие на дофаминергические рецепторы постсинаптической мембраны и вызывает её деполяризацию. Предполагается, что около 80% дофамина поглощается обратно в пресинаптическое пространство или инактивируется при помощи фермента КОМТ (катехол –О-метилтрансферазы) или МАО-В (моноаминооксидазы типа В). Наиболее вероятными механизмами повреждения нейронов при БП являются: окисдативный стресс; повышенное содержание ионов железа; выявлены специфичные ферментативные дефекты комплекса I дыхательной цепи в митохондриях черной субстанции; индукция процессов апоптоза, вследствие эксайтотоксического влияния глутамата и аспартата. Но реальный пусковой фактор этих процессов до конца не определен. Помимо дофаминергических нейронов черной субстанции при болезни Паркинсона дегенерации подвергаются и другие группы нейронов, в том числе нейроны дорсального ядра блуждающего нерва, нейроны обонятельной луковицы, норадренергические нейроны голубого пятна, серотонинергические нейроны ядер шва, холинергические нейроны ядра Мейнерта, а также нейроны коры больших полушарий и некоторые вегетативные сплетения. В силу этого, помимо дефицита дофамина, возникает дисфункция серотонинергических, норадренергических и холинергических систем. С поражением экстранигральных структур связаны такие проявления болезни, как аносмия, вегетативная недостаточность, депрессия, деменция.
Клинические проявления.
Болезнь Паркинсона начинается постепенно, медленно прогрессирует. От момента появления первых неспецифических (домоторных проявлений таких как: констипация, нарушения сна, потеря обоняния, депрессия, расстройство поведения в фазе быстрого сна) до основных двигательных симптомов проходит 10-15 лет. Первые двигательные симптомы БП появляются когда гибнет более 50 % нейронов черной субстанции, а снижение уровня дофамина составляет до 80 %.
| Премоторная симптоматика | Связь со структурами головного мозга | Стадия по Брааку |
| Констипация (запор) | Дорсальное ядро вагуса; нейроны брюшного сплетения. | 1 |
| Нарушение сна или потеря обоняния | Обонятельная луковица; переднее ольфакторное ядро | 1 |
| Депрессия | Голубоватое место, ядра шва. | 2 |
| Расстройство поведения в фазе быстрого сна (REM) | Дорзальная часть среднего мозга и мост; голубоватое место. | 2 |
| Акинезия | Черное вещество. | 3 |
Основными в клинической картине являются двигательные симптомы:
- Снижение двигательной активности (гипокинезия). Основные проявления гипокинезии – затруднения при выполнении «мелких» движений (застегивание пуговиц, завязывание шнурков, нарезка продуктов, чистка зубов); шаркающая походка, затруднения при поворотах в постели, вставании со стула; изменение речи (снижение модуляций и эмоциональной окраски голоса, который становится маловыразительным, монотонным, затухающим); изменение почерка – микрография (почерк становится мелким, буквы связаны, размер их уменьшается к концу предложения); амимия – маскообразное лицо, бедная мимика; «поза прсителя» — шея, туловище и конечности в суставах несколько согнуты, прижаты к туловищу; пропульсия, ретропульсия, латеропульсия – непреодолимое ускорение движения больного вперед, назад, в сторону при ходьбе или после легкого толчка, невозможность остановить начатое движение или изменить направление; ахейрокинез – отсутствие содружественных движений рук при ходьбе; парадоксальные кинезии – у больных, едва передвигающихся с посторонней помощью и лежачих — возможность быстрых движений (бегать, прыгать, вальсировать и т.д.) под воздействием эмоциональных факторов.
- Повышение мышечного тонуса (ригидность) – ощущается как «скованность», напряженность мышц (феномен «восковой куклы», феномен «зубчатого колеса» — возникают когда на ригидность накладывается тремор)
- 3. Тремор покоя (у 80% пациентов) по типу «скатывания пилюль», «счета монет» — ритмичное дрожание дистальных отделов рук, особенно пальцев, малой амплитуды и частоты, прекращающийся во время целенаправленных движений и исчезающий во время сна.
- Нарушение равновесия (постуральная неустойчивость)
БП проявляется клинически не только двигательными нарушениями, но и имеет целый спектр недвигательных проявлений, которые встречаются у всех пациентов независимо от возраста дебюта заболевания и стадии болезни:
- Когнитивные нарушения
- Аффективные нарушения (депрессия, тревога, апатия, обсессивно-компульсивный синдром)
- Поведенческие нарушения (пристрастие к азартным играм, компульсивный шоппинг, гиперсексуальность, булимия)
- Психические нарушения (галлюцинации, бред, делирий)
- Нарушения сна (инсомния, гиперсомния, парасомния)
Вегетативные нарушения при БП:
- Ортостатическая гипотензия
- Сальность покровов головы, повышенное образование ушной серы.
- Сиалорея
- Потливость
- Дистальный гипергидроз
- Нарушение мочеиспускания
- Запоры
- Вагоинсулярные кризы
Классификация.
Классификация болезни Паркинсона проводится по форме, стадии и темпу прогрессирования заболевания. Формы заболевания. В зависимости от преобладания в клинической картине того или иного симптома выделяют следующие формы: смешанную (акинетико-ригидно-дрожательную), акинетико-ригидную и дрожательную. Смешанная форма выявляется в 60–70 % случаев болезни Паркинсона, акинетико-ригидная — в 15–20 % случаев болезни Паркинсона, дрожательная — в 5–10 % случаев болезни Паркинсона. По мере прогрессирования заболевания его форма может меняться.
Стадии заболевания. Общепризнанной является классификация стадий болезни Паркинсона, предложенная Hoehn и Yarh (1967): 1 стадия – Гемипаркинсонизм (односторонние проявления) 1,5 стадия – односторонние проявления с вовлечением аксиальной мускулатуры. 2 стадия – Двусторонние нарушения без нарушения равновесия. 2,5 стадия – Двусторонние нарушения с начальными проявлениями постуральной неустойчивости, но с самостоятельным восстановлением равновесия при толчковой пробе. 3 стадия – Двусторонние нарушения с присоединением постуральных нарушений. 4 стадия – Выраженные нарушения, но может стоять и ходить без посторонней помощи 5 стадия – полная инвалидизация. Больной прикован к постели или к инвалидному креслу.
Темп прогрессирования.
Выделяют три варианта темпа прогрессирования болезни Паркинсона (при условии адекватного лечения):
- быстрый темп прогрессирования, при котором смена стадий заболевания (первая — вторая или вторая — третья) происходит в течение 2 или менее лет;
- умеренный темп прогрессирования, при котором смена стадий происходит более чем за 2 года, но не более чем за 5 лет;
- медленный темп прогрессирования со сменой стадий более чем через 5 лет.
Диагностика.
В настоящее время для клинической диагностики болезни Паркинсона чаще всего используют критерии банка головного мозга Общества болезни Паркинсона Великобритании (A. Hughes et al., 1992). Гипокинезия в сочетании не менее чем с одним из следующих симптомов:
- мышечная ригидность;
- тремор покоя с частотой 4-6 ГЦ;
- постуральная неустойчивость.
Критерии исключения болезни Паркинсона:
- повторные инсульты в анамнезе со ступенеобразным прогрессированием симптомов паркинсонизма;
- повторные черепно-мозговые травмы в анамнезе;
- энцефалит в анемнезе;
- окулогирные кризы;
- лечение нейролептиками на момент появления симптомов;
- семейный характер заболевания (более 1 родственника с аналогичным заболеванием);
- наличие длительной ремиссии;
- строго односторонняя симптоматика более 3 лет;
- паралич взора вниз;
- ранняя быстро прогрессирующая вегетативная недостаточность;
- мозжечковые знаки;
- рано развивающаяся деменция с нарушениями памяти, речи, праксиса;
- симптом Бабинского;
- наличие атрофии мозжечка или сообщающейся гидроцефалии на компьютерной томографии;
- отсутствие реакции на высокие дозы леводопы (при исключении мальабсорбции);
- контакт с токсическими веществами, вызывающими паркинсонизм.
Критерии, подтверждающие диагноз болезни Паркинсона (не менее 3):
- одностороннее начало;
- тремор покоя;
- прогрессирующее течение;
- сохранение асимметрии симптоматики с преобладанием на первоначально вовлеченной стороне;
- высокая эффективность препаратов леводопы (уменьшение симптомов на 70–100 %);
- выраженные хореиформные дискинезии, индуцированные леводопой;
- сохранение реакции на леводопу в течение 5 лет и более;
- продолжительность заболевания в течение 10 лет и более.
Дифференциальная диагностика болезни Паркинсона проводится со следующими заболеваниями: эссенциальный тремор, юношеский (ювенильный) паркинсонизм, лекарственный паркинсонизм, сосудистый паркинсонизм, прогрессирующий надъядерный паралич (синдром Стила — Ричардсона — Ольшевского), мультисистемная атрофия, болезнь диффузных систем Леви, гепатолентикулярная дегенерация.
Дополнительные методы исследования.
- Структурная нейровизуализация – КТ, МРТ – малоинформативны для диагностики БП и используются для исключения вторичного паркинсонизма.
- Функциональная нейровизуализация (ПЭТ с флюородопой, ОФЭКТ) возможность этих методов высока, т.к. позволяют выявить изменения дофаминового обмена за 4-6 лет до появления клинических симптомов, но в данный момент это является технически сложным и дорогим методом исследования, что не позволяет использовать его в рутинной практики для выявления БП.
- Транскраниальная сонография – выявляет повышенную гиперэхогенность черной субстанции, за счет повышенного содержания трехвалентного железа, которые выявляются у 80-90 % пациентов с БП.
- Обонятельные тесты (Пенсильванский тест) Обонятельная дисфункция это наиболее ранний домоторный признак БП. Наиболее часто используется это тест, если в клинике преобладает дрожание, проводя дифференциальную диагностику между эссенциальным тремором и БП, потому что только для идиопатического паркинсонизма будет характерно изменение обонятельных тестов.
Принципы лечения.
В лечении болезни Паркинсона можно выделить три основных направления:
- Нейропротекторная терапия, целью которой является замедлить или остановить дегенерацию нейронов головного мозга. В последние годы экспериментальные и клинические испытания прошли несколько десятков средств, потенциально способных влиять на различные стадии нейродегенеративного каскада гибели клеток (антиоксиданты, антагонисты глутамата, блокаторы кальциевых каналов, противовоспалительные средства, трофические факторы и т.д.), однако пока их эффективность доказать не удалось.
- симптоматическая терапия, позволяющая уменьшить основные симптомы заболевания за счет коррекции возникающего в мозге нейрохимического и нейрофизиологического дисбаланса;
- физическая и социально-психологическая реабилитация.
Медикаментозное лечение.
В настоящее время лечение проводят, ориентируясь главным образом на симптоматический эффект препаратов. На данный момент к числу противопаркинсонических средств, применяемых при болезни Паркинсона, относят 6 групп лекарственных средств:
- препараты, содержащие леводопу (предшественника дофамина) — обеспечивают повышение синтеза дофамина в мозге;
- агонисты дофаминовых рецепторов – стимуляция рецепторов чувствительных к дофамину;
- трициклические антидепрессанты – торможение процесса обратного поглащения (захвата) дофамина пресинаптическими структурами;
- препараты амантадина – стимуляция процесса выброса (высвобождения) дофамина из пресинаптической терминали;
- ингибиторы моноаминооксидазы типа В;
- ингибиторы катехол-О-метилтрансферазы – торможение катаболизма (распада) дофамина;
Поскольку механизм действия препаратов этих групп различен, при необходимости их можно сочетать в рамках комбинированной терапии.
Медикаментозная терапия пациентов с болезнью Паркинсона подбирается индивидуально для каждого клинического случая и зависит от ряда факторов, в том числе от выраженности функциональной недостаточности, формы заболевания, возраста больного, индивидуальной чувствительности к препаратам, фармакоэкономических соображений.
Задачей терапии является восстановление нарушенных двигательных функций при использовании минимальных эффективных доз препаратов. В течение первых месяцев болезни, когда проявления заболевания минимальны и не нарушают повседневной социальной или бытовой активности, лекарственная терапия может не назначаться. В начале лечения обычно прибегают к монотерапии, а в случае снижения ее эффективности при прогрессировании болезни — к комбинированной терапии.
Немедикаментозные методы лечения.
Лечение хронических заболеваний наряду с назначением лекарственных средств требует осуществления мер по социально-психологической поддержке больных. Образовательные программы должны предоставлять больным выборочную информацию о заболевании, необходимую для формирования у них ощущения контроля над болезнью. В комплекс лечения должны входить нейропсихологический тренинг, речевая терапия, лечебная гимнастика. Регулярные физические занятия, включающие аэробные упражнения, упражнения в изометрическом режиме, на растяжение и координацию, способны, не уменьшая паркинсонических симптомов, улучшить подвижность больных. Важное значение имеет полноценное питание, позволяющее предотвратить снижение веса и утрату мышечной массы. Для осуществления всего комплекса мер по медико-социальной реабилитации больных целесообразно создать специальную службу. Необходима подготовка специально обученных средних медработников, которые координировали бы работу социальных служб, обучали родственников приемам ухода, занимались образованием больных.
Нейрохирургическое лечение.
При неэффективности консервативной терапии, особенно когда выраженные дискинезии не позволяют назначать дозы препаратов леводопы, необходимые для коррекции симптомов болезни Паркинсона, ставится вопрос об оперативном лечении (паллидотомия, таламотомия, вживление внутримозговых стимуляторов в бледный шар, таламус, субталамическое ядро, внутримозговая трансплантация эмбриональной ткани надпочечника или черной субстанции).
Методы диагностики
Поставить диагноз только по наличию клинических признаков затруднительно, поскольку проявления сосудистого паркинсонизма могут отличаться. Более подробная диагностика необходима для подтверждения данных первичного осмотра, а также для выяснения причины патологического процесса. Она может включать следующие методики:
- осмотр невролога — на данном этапе можно установить мышечную ригидность, особенно на нижних конечностях, различные неврологические расстройства, а также снижение интеллектуального развития;
- ультразвуковая диагностика сосудов шеи и головы — проводится для оценки скорости кровотока, а также для исключения тромбозов, сужения сосудистых стенок и других органических изменений;
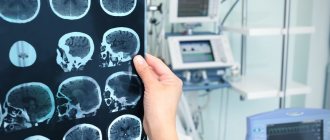
- магнитно-резонансная томография головного мозга — наиболее информативный способ диагностики нервной системы, на снимках будут отчетливо видны участки, поврежденные инсультом.
Для более детальной диагностики можно использовать и дополнительные методики. К ним относится ПЭТ (позитронно-эмиссионная томография) и другие способы, которые позволяют получить наиболее подробную картину болезни. Однако из-за высокой стоимости и сложности проведения процедуры они применяются редко. Для постановки диагноза достаточно простого осмотра, УЗИ сосудов и МРТ головного мозга.
Поставить окончательный диагноз на основании данных первичного осмотра невозможно — понадобится комплексное обследование
Тактика лечения
Лечение сосудистого паркинсонизма комплексное и включает применение нескольких групп препаратов. Их необходимо принимать курсом, поскольку полностью восстановить функции нервной системы не получится. Их действие направлено на стабилизацию состояния больного, снижение частоты рецидивов, улучшение координации движений и сохранение уровня интеллектуального развития.
Первый этап — это базисная терапия. Она подразумевает прием препаратов для улучшения церебрального кровообращения. По необходимости назначают антикоагулянты — средства, которые разжижают кровь и препятствуют появлению тромбов.
Второй этап — это симптоматическое лечение. Препараты, которые назначаются против сосудистого паркинсонизма, подбираются индивидуально:
- противопаркинсонические средства — вызывают положительную динамику у 30—50% пациентов;
- ноотропы — вещества для активации мозговой активности;
- антидепрессанты;
- обезболивающие средства.
Последний этап — это лечебная физкультура. Тренировки проводятся в домашних условиях и включают простые упражнения для повышения силы и эластичности мышц. Также полезно выполнять задачи на развитие координации движений.
Лечение
Раннее начало заболевания накладывает свой отпечаток и на тактику лечения — его необходимо планировать на десятилетия вперед. Обычно терапию начинают с назначения агонистов дофаминовых рецепторов. Во-первых, эти препараты лучше переносятся молодыми людьми по сравнению с пожилыми больными в классических случаях. А во-вторых, при назначении стандартного лечения «Леводопой» у молодых быстро развивается дискинезия — непроизвольные сокращения мышц. И возникает парадоксальная ситуация, когда у одного пациента имеется и мышечная слабость, и патологическое сокращение мышц. Также используются «Амантадин», ингибиторы МАО-В, ингибиторы КОМТ, холинолитики. Но рано или поздно все равно встанет вопрос о необходимости назначения «Леводопы» как наиболее эффективного на сегодняшний день медикаментозного метода лечения. Для того чтобы минимизировать риски осложнений (гиперкинезы), подбирается индивидуальная дозировка препарата и проводится его титрование.
Также все шире применяются хирургические способы лечения болезни Паркинсона. В частности, проводится высокочастотная электростимуляция базальных ганглиев, установка помп, которые позволяют поддерживать постоянную концентрацию препарата в крови.
Возможные осложнения и прогноз
Постепенное прогрессирование болезни приводит к снижению способности пациента к самообслуживанию. Расстройства мозговой деятельности становятся причиной деменции — приобретенного слабоумия. Однако наиболее опасен псевдобульбарный паралич — нарушение мышечной активности вследствие отсутствия ее иннервации. У таких пациентов остается риск аспирации (вдыхания) пищи и развития аспирационной пневмонии — воспаления легких. Прогноз зависит от причины и тяжести течения болезни, возраста больного и других факторов.