Синдром вертебральной (позвоночной) артерии является определением группы синдромов (сосудистых, вегетативных) возникающих вследствие нарушения кровотока в вертебральных артериях, вызванных различными проблемами. Основными этиологическими причинами развития синдрома вертебральной артерии служат следующие заболевания.
- Сосудистые заболевания с нарушением проходимости сосудов, такие как атеросклероз, различные артриты эмболии.
- Изменение формы артерий (деформации) – ненормальная извитость, значительные перегибы, аномальные структурные изменения артерий.
- Экстравазальная компрессия сосудов (компрессия артерий остеофитами, грыжами, протрузиями дисков, компрессия костными аномалиями, опухолями, рубцовой тканью)
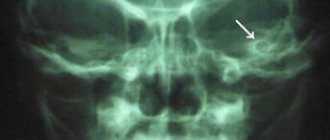
Учитывая, что причиной синдрома могут различные факторы, иногда возникают трудности с трактовкой такого диагноза, как синдром вертебральной артерии, так как этим синдромом можно обозначить самые различные состояния, например, такие как острые нарушения кровообращения. Но в клинической практике наибольше значение имеют дегенеративно-дистрофические изменения в шейном отделе позвоночника и аномальные явления со стороны атланта, которые приводят к нарушению кровотока в бассейне вертебральных артерий и появлению симптомов нарушения мозгового кровообращения.
Различают экстракраниальный и интракраниальный отделы позвоночной артерии.
Значительная часть экстракраниального отдела позвоночные артерии проходят через подвижный канал образованный отверстиями в поперечных отростках позвонков. Через этот канал проходит также симпатический нерв (нерв Франка). На уровне С1-С2 позвоночные артерии закрываются только мягкими тканями. Такая анатомическая особенность прохождения позвоночных артерий и мобильность шейного отдела значительно увеличивают риск развития компрессионного воздействия на сосуды со стороны окружающих тканей.
Возникающая компрессия со стороны окружающих тканей приводит к компрессии артерии вегетативных окончаний и констрикции сосудов вследствие рефлекторного спазма, что приводит к недостаточному кровоснабжению головного мозга.
Дегенеративные изменения в шейном отделе (остеохондроз, артроз фасеточных суставов, унковертебральный артроз, нестабильность двигательных сегментов, грыжи дисков, деформирующий спондилез, костные разрастания (остеофиты), мышечные рефлекторные синдромы (синдром нижней косой мышцы, синдром передней лестничной мышцы)- являются нередко причиной компрессии позвоночный артерий и развития синдрома вертебральной артерии. Чаще всего, компрессия возникает на уровне 5-6 позвонков, чуть реже на уровне 4-5 и 6-7 позвонков. Наиболее частой причиной развития синдрома позвоночной артерии является унковертебральный синдром. Близкое расположение этих сочленений к позвоночным артериям приводит к тому, что даже небольшие экзостозы в области унковертебральных сочленений приводят к механическому воздействию на позвоночные артерии. При значительных унковертебральных экзостозах возможно значительное сдавление просвета вертебральных артерий.
Достаточно значимую роль в развитии синдрома вертебральной артерии играют аномалии Кимберли, Пауэрса.
1.Общие сведения
Кохлеарный неврит – собирательный диагноз, обобщающий состояния тугоухости вследствие поражения слухового нерва; широко употребляются также (в одних случаях как синоним, в других – как обозначение осевого симптома) термины «нейросенсорная тугоухость» и «сенсоневральная тугоухость».
В отличие от абсолютного большинства диагнозов с окончанием на «-ит», кохлеарный неврит не подразумевает доминирующего этиопатогенетического значения инфекционно-воспалительных процессов. Некоторые авторы, определяя объем и содержание данного понятия, вообще настаивает на неинфекционном характере поражения; в других источниках вуалируется значение воспалительного фактора, и т.д. Вообще говоря, формулировка «кохлеарный неврит» относится к тем диагнозам, которые воспринимаются и интерпретируются (даже специалистами) больше на интуитивном, чем на рациональном уровне. Англоязычный термин «Auditory neuropathy» (слуховая невропатия) представляется несколько более удачным.
Так или иначе, тугоухость, обусловленная поражениями слуховых нейронных проводников, широко распространена: согласно современным данным, это наиболее частая причина частичной или полной утраты слуха. При этом эпидемиологические оценки, публикуемые в разных источниках, существенно расходятся. В первом приближении и с учетом сводок ВОЗ, общее количество тугоухих в мире составляет не менее 300 млн чел. По другим сведениям, этот показатель еще выше и достигает 10% населения земного шара, из которых фактическими инвалидами являются 125 миллионов человек (три четверти из них – жители беднейших стран). По России число социально-значимой тугоухости оценивается на уровне 13 млн чел, при этом как минимум миллион приходится на лиц детского и подросткового возраста.
Таким образом, частичная или полная утрата слуха – одна из глобальных проблем здравоохранения, и ее острота драматически усугубляется тем, что на сегодняшний день не существует подлинно эффективных способов лечения кохлеарного неврита как доминирующего этиопатогенетического фактора тугоухости.
Обязательно для ознакомления! Помощь в лечении и госпитализации!
Ишемические кохлеовестибулярные синдромы (ИКВС) — сочетание вестибулярных нарушений (головокружение, неустойчивость) с шумом в ушах и снижением слуха. ИКВС являются одной из наиболее частых форм головокружения и развиваются при недостаточности кровообращения в артериях, кровоснабжающих внутреннее ухо, корешок VIII нерва, вестибулярные ядра и их проводящие пути [1]. Как правило, развитие ИКВС обусловлено нарастающими проявлениями ишемии головного мозга [6, 7].
Различают периферический и центральный ИКВС. Периферический связан с недостаточностью кровообращения в мелких артериях, кровоснабжающих лабиринт и VIII нерв [2, 14]. Центральный ИКВС возникает в результате ишемии вестибулярных ядер ствола мозга [11, 17].
В редких случаях изолированное вестибулярное головокружение может быть обусловлено острым нарушением мозгового кровообращения при окклюзии дистальной ветви передней нижней мозжечковой артерии, вызывающей ишемию клочка мозжечка, окклюзии ветвей задней нижней мозжечковой артерии или окклюзии артерии лабиринта [5].
Механизмы риска развития ИКВС
Основными механизмами развития ИКВС являются атеросклеротическое поражение экстра- и интракраниальных сосудов головного мозга, артериальная гипертензия (АГ), выраженная деформация позвоночных артерий (ПА), аномалии артерий вертебрально-базилярной системы (ВБС), нарушения состояния системы гемостаза, артерио-артериальная и кардиальная эмболия, тяжелые нарушения центральной гемодинамики [10, 11].
Атеросклероз церебральных артерий принято считать наиболее частой причиной ИКВС. Атеросклеротический процесс вызывает нарушение мозгового кровообращения вследствие формирования стенозов или окклюзий магистральных артерий головы и/или интракраниальных артерий, ухудшения коллатерального перераспределения крови, увеличения мозгового периферического сосудистого сопротивления, снижения церебральной перфузии, кислородного и энергетического голодания ткани мозга [7]. Следует отметить, что с возрастом снижаются адаптационные возможности пациентов как к экзогенным, так и эндогенным воздействиям. Более половины всех ишемических инсультов у пожилых в той или иной степени связаны с поражением экстрацеребральных артерий, прежде всего, атеросклеротического генеза. У 50% больных старше 60 лет атеросклероз сочетается с АГ [10].
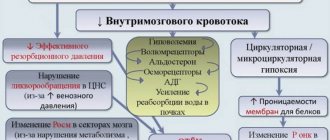
Поражение головного мозга при АГ обусловлено комплексом таких нарушений, как извитость сонных и ПА, утолщение комплекса интима-медиа, дисфункция эндотелия, нарушения цереброваскулярной реактивности. При этом происходят репаративные и адаптивные процессы, развивается гипертрофия мышечной оболочки экстрацеребральных сосудов с появлением «гипертонических стенозов» и последующей облитерацией просвета. Перекалибровка артерий приводит к редукции мозгового кровотока и ишемии мозговой ткани [3—5]. Анатомические особенности кровоснабжения головного мозга таковы, что при неконтролируемой АГ в первую очередь страдают глубинные отделы белого вещества головного мозга, подкорковые базальные ядра и мозжечок. Указанные отделы головного мозга наиболее часто являются областью локализации лакунарных инфарктов. Патоморфологические исследования венозной системы головного мозга при АГ свидетельствуют о ее выраженных нарушениях, вплоть до облитерации венозных синусов мозга. Возникают изменения сосудистой стенки с повышением ее проницаемости, перивентрикулярным отеком, вторичным сдавлением венул, замедлением венозного оттока [1, 24]. Нарушается и состояние микроциркуляции — ухудшается деформируемость тромбоцитов, повышается гематокрит, увеличивается вязкость крови.
Помимо органического поражения экстра- и интракраниальных сосудов существует так называемый стрессогенный патогенетический вариант развития ИКВС,
обусловленный, главным образом, истощением возможностей энергетического обмена и ухудшением кровообращения в мозге в результате перенапряжения церебральных систем на фоне длительного воздействия на них активирующих безусловно- и условно-рефлекторных стимулов [9].
Дегенеративно-дистрофические заболевания позвоночника также могут привести к возникновению ИКВС вследствие нарушения состояния периваскулярных сплетений и нижнего шейного симпатического узла, обеспечивающих симпатическую иннервацию ПА [3, 16]. Возможность поражения ПА при дегенеративных поражениях шейного отдела позвоночника определяется ее топографо-анатомическими особенностями. Значительная часть экстракраниального отрезка ПА находится в подвижном костном канале, проходящем в поперечных отростках шейных позвонков. В этой области боковая стенка ПА прилежит к унковертебральному сочленению, а задняя соседствует с верхним суставным отростком. На уровне СI-СII ПА прикрыта лишь мягкими тканями, преимущественно нижней косой мышцей головы. В физиологических условиях, при сдавлении и ограничении кровотока в одной из артерий, поступление крови к головному мозгу обычно не нарушается в силу достаточных компенсаторных возможностей. Положение меняется при гипоплазии или наличии атеросклеротического стеноза одной из ПА. В этой ситуации экстравазальные факторы (компрессия суставными отростками при нестабильности шейного отдела позвоночника или остеофитами в унковертебральных областях и др.) становятся основными причинами недостаточности кровообращения в ВБС. Считается, что именно остеофиты оказывают наибольшее компрессирующее влияние на ПА, они могут вызывать ирритацию симпатического сплетения лишь при определенных положениях или движениях в шейном отделе позвоночника. Кроме механической компрессии возможен спазм сосуда в результате раздражения периартериального нервного сплетения. Смещение и компрессия ПА могут наблюдаться и в результате подвывиха суставных отростков позвонков. Кроме того, вследствие патологической подвижности отдельных позвоночных двигательных сегментов шейного отдела позвоночника, ПА может травмироваться верхушкой верхнего суставного отростка нижележащего позвонка [23, 25]. Также возможно сдавление ПА мышцами шеи (лестничными, длинной мышцей шеи, нижней косой мышцей головы) при определенных положениях головы. Наиболее часто ПА оказывается сдавленной в области между V и VI шейными позвонками, несколько реже — между IV и V, VI и VII позвонками [26]. Из-за близости ПА к атлантоаксиальному сочленению, где общее фасциальное влагалище сосудисто-нервного пучка прилегает к наружному слою его капсулы, возможно уменьшение кровотока по ПА при боковом наклоне или ротации зуба аксиса [9, 28]. Выйдя из поперечного отростка атланта, ПА направляется назад горизонтально и ложится в борозду ПА. У части людей над бороздой образуется костный мостик — аномалия Киммерле, способная оказывать компрессионно-ирритативный эффект с резким снижением кровотока в ПА. Как правило, в клинической практике ИКВС развиваются при смешанных (компрессионно-ирритативных) вариантах поражения ПА.
Патогенез ИКВС
В основе ИКВС лежат нарушения гемодинамики, влекущие за собой разные формы функциональных нарушений вестибулярной системы. Патогенетической базой ИКВС являются ишемия, нарушения трофики рецепторов лабиринта и связанных с ним структур головного мозга и метаболизма в них вследствие сосудистого поражения головного мозга [14, 15, 18, 19]. Эти нарушения определяются совокупностью факторов: состоянием метаболизма в ткани мозга, напряжением кислорода (pO2), углекислого газа (рСО2), кислотно-основным состоянием и рН ткани мозга, уровнем системного артериального давления, локальной нейрогенной регуляцией сосудистого тонуса, включающей импульсы из сосудодвигательного центра разных отделов ствола мозга и гипоталамуса, из нервного сплетения барабанной полости [1].
В зависимости от характера изменений сосудистого русла зона ишемии может локализоваться как на периферии (в лабиринте), так и в других отделах головного мозга, что клинически, помимо иных симптомов, может проявляться периферическим или центральным ИКВС. Можно предположить, что в патогенезе острого ИКВС играет роль затруднение венозного оттока из поперечного синуса при гипертоническом кризе в результате открытия артериоло-венозных шунтов. Нередко у таких пациентов выявляется вторичный гидропс лабиринта, обусловленный нарушением кровообращения внутреннего уха на фоне нарушения венозного оттока из полости черепа. Расстройства ликвородинамики усугубляются повышением основных параметров перекисного окисления липидов, снижением эффективности функционирования антиоксидантной системы, гиперкоагуляцией и гиперагрегацией тромбоцитов, нарушениями липидного обмена.
В основе развития цереброваскулярных заболеваний лежат изменения метаболизма и трофики нейронов и дисфункция нейромедиаторных систем [22, 24]. Нарушения метаболических и белоксинтетических процессов в нейронах лежат в основе нейродегенеративного поражения, являющегося основой дальнейшего прогрессирования заболевания. Не меньшее значение имеют и нарушения функционирования нейромедиаторных систем, регуляции сосудистого тонуса, снижающие адаптационные возможности сосудистого русла.
Клинические проявления ИКВС
Для периферического ИКВС характерны острое начало, резко выраженное системное головокружение, сопровождающееся тошнотой, рвотой, иногда — утратой сознания, в сочетании с односторонним снижением слуха, ощущением шума в ухе, нистагмом. В ряде случаев нарушения слуха выражены незначительно и проявляются только нарушением разборчивости речи. Для центрального ИКВС характерны подострое начало, сочетанный — системный и несистемный характер головокружения, постепенное двустороннее снижение слуха или ощущение шума в ушах, двусторонний нистагм. Характерны затылочные головные боли, иногда иррадиирующие в шею, теменно-височную область и глазницы, неустойчивость при ходьбе и стоянии (статическая атаксия), реже — динамическая атаксия. Возможны приступы внезапного падения без потери сознания («дроп-атаки»), синкопальные состояния. У отдельных пациентов имеют место зрительные и глазодвигательные расстройства в виде преходящей диплопии, фотопсий, преходящей гемианопсии. Нередкими являются снижение памяти на текущие события, приступы транзиторной глобальной амнезии, когда на несколько часов у больного нарушается способность к запоминанию при сохранной способности к осуществлению целенаправленных действий. В определенной степени это состояние имеет сходные черты с корсаковским синдромом и связано с преходящей ишемией медиобазальных отделов височных и теменно-затылочных долей мозга [13].
Клинические проявления ИКВС имеют возрастные особенности. В пожилом и старческом возрасте нередко наблюдаются множественность и повторяемость острых эпизодов острой ишемии в ВБС. Клинически это проявляется приступами головокружения, нистагмом, нарушениями равновесия и координации. Результаты проведенного исследования [22] убедительно доказывают, что вертебрально-базилярная недостаточность — сравнительно редкая причина головокружения у пожилых. В 17,1% случаев головокружение обусловлено обратимым нарушением мозгового кровообращения в ВБС и повреждением центральных вестибулярных структур, и только у 5,7% пациентов является следствием перенесенного острого нарушения мозгового кровообращения, что было подтверждено нейровизуализационными исследованиями и вестибулометрией. У 8 (11,4%) больных постуральные нарушения были обусловлены хронической недостаточностью мозгового кровообращения. Это связано с тем, что в пожилом возрасте трудно выделить единственную ведущую причину развития ИКВС. Как правило, они множественные — гиперхолестеринемия, извитость одной или обеих ПА, атеросклеротический стеноз внутренних сонных артерий, наличие дегенеративно-дистрофических изменений в позвоночнике [10].
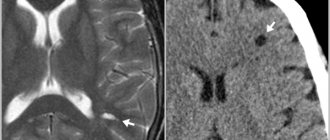
Важным проявлением хронической ишемии головного мозга является изменение белого вещества (лейкоареоз) глубинных отделов мозга. У пожилых пациентов зафиксирована связь между распространенностью лейкоареоза, особенно в передних отделах мозга, локализацией лакунарных очагов в чечевицеобразном ядре и выраженностью нарушений ходьбы и равновесия, когнитивными расстройствами (КР) [29]. Правильная постановка диагноза ИКВС у пациентов с КР бывает затруднена [31]. У 25—30% больных после перенесенного инсульта в течение года развивается деменция. До 30—70% больных, перенесших инсульт, страдают умеренными КР, что затрудняет сбор анамнеза и правильную интерпретацию жалоб.
Диагностика и дифференциальная диагностика ИКВС
Диагностика ИКВС — непростая задача. С одной стороны, головокружение при различных заболеваниях может протекать абсолютно одинаково, с другой, — иметь различную клиническую картину при одном виде патологии. Например, у амбулаторных пациентов с головокружением причина заболевания бывает установлена только в 20% случаев [7]. При постановке диагноза необходимо провести тщательное обследование пациента, включающее детальный сбор анамнеза и анализ жалоб. Важное значение имеет измерение артериального давления в положении лежа и стоя — при значительном снижении систолического давления (более 20 мм рт.ст.) в вертикальном положении, сопровождающемся симптоматикой, клинические проявления, сходные с вертебрально-базилярной недостаточностью, следует рассматривать как следствие ортостатической гипотензии. При неврологическом обследовании следует обращать внимание на наличие или отсутствие нистагма, статической или динамической атаксии. Значительную ценность имеют результаты проб Ромберга (больной, стоя с закрытыми глазами, отклоняется в сторону поражения лабиринта) и Бабинского—Вейля (больной с закрытыми глазами делает несколько раз пять шагов вперед и назад — при одностороннем вестибулярном поражении его маршрут будет иметь форму звезды). У пожилых пациентов и пациентов, злоупотребляющих алкоголем, токсическими веществами, наркотиками необходимо проводить нейропсихологическое тестирование с целью выявления КР. В диагностический алгоритм входит также отоневрологическое обследование, включающее компьютерную электронистагмографию (КЭНГ), аудиометрию, регистрацию слуховых вызванных потенциалов (СВП). При подозрении на спондилогенное влияние на ПА проводят рентгенографию или МРТ шейного отдела позвоночника, дуплексное сканирование ПА. Дифференциальная диагностика ИКВС должна проводиться с учетом характерных особенностей болезни Меньера, демиелинизирующих заболеваний центральной нервной системы, опухолей мостомозжечкового угла.
Приступ болезни Меньера похож на приступ при ИКВС, но по продолжительности значительно короче, течение болезни рецидивирующее. Характерно, что внезапный приступ интенсивного системного головокружения в сочетании с тошнотой и рвотой, спонтанным нистагмом, односторонним снижением слуха полностью купируется на протяжении 1—3 ч. При обследовании отсутствуют какие-либо другие неврологические симптомы.
У больных рассеянным склерозом могут наблюдаться головокружение и другие симптомы, характерные для ИКВС. Заболевание имеет ремиттирующий характер, для него характерно сочетание вестибулярных и мозжечковых нарушений с признаками поражения других отделов центральной нервной системы, наличие очагов демиелинизации белого вещества при МРТ головного мозга. Для опухолей мостомозжечкового угла характерны нарушение слуха (одностороннее резкое снижение слуха), явления вестибулярной дисфункции при отсутствии головокружения, признаки поражения расположенных вблизи черепных нервов.
Принципы терапии
Несмотря на то, что многим пациентам, страдающим головокружением, можно оказать эффективную помощь, лечение нередко оказывается неадекватным [12]. Не вызывает сомнения, что лечение больных с ИКВС, в первую очередь, должно быть направлено на устранение вызвавшей их причины, однако причины не всегда могут быть выявлены и легко устранены. В связи с этим существенное значение имеет симптоматическое лечение. Предлагаемые на сегодняшний день лекарственные препараты для лечения пациентов с ИКВС относятся к разным фармакологическим группам и имеют различную эффективность и переносимость. До сих пор нет четкой картины в понимании механизмов вестибулолитического действия наиболее широко используемых препаратов.
Главными целями терапии являются предотвращение возникновения или прогрессирования патологического процесса, улучшение когнитивных функций и общетерапевтические меры [27, 28]. Основным вопросом медицинской практики является поиск «идеального» лекарственного средства или комплекса препаратов и соблюдение требований к их использованию. Терапия ИКВС должна быть комплексной, включать препараты с разновекторным механизмом действия. Для профилактики вторичных ишемических нарушений требуется назначение антиагрегантов (ацетилсалициловая кислота, тиклопидин), а при нарастании симптоматики — антикоагулянтов [20]. Лечение системного головокружения во многом определяется его причиной, кроме того, важную роль играет симптоматическая терапия [30]. Следует четко разграничивать так называемую скоропомощную и длительную терапию [21].
Необходимо раннее назначение и длительное использование вестибулолитических препаратов. Например, препараты бетагистина дигидрохлорида, обладающие воздействием на гистаминовые Н1- и H3-рецепторы и улучшающие микрогемоциркуляцию в лабиринте и нейротрансмиссию в области вестибулярных ядер ЦНС[4]. Бетагистин является препаратом, который способствует накоплению и выделению гистамина в нейрональных синапсах центральной и периферической нервной системы, но при этом лишен побочных эффектов гистамина. На периферии данный препарат увеличивает микроциркуляцию во внутреннем ухе, улучшает кохлеарный кровоток. Центральные гистаминовые рецепторы под воздействием бетагистина получают возможность компенсации и ускорения вестибулярной адаптации. Препарат оказывает прогистаминовый эффект на постсинаптической мембране, преимущественно влияя на H3-рецепторы, расположенные на пресинаптической мембране. Головокружение блокируется за счет агонистических воздействий препарата на центральные и периферические рецепторы H1. При этом бетагистин не влияет на H2-рецепторы желудочно-кишечного тракта. Использование этого лекарственного средства не дает быстрый клинический эффект, требует соблюдения режима дозирования (суточная доза 48 мг) и длительного приема (не менее 1 мес).
«Скоропомощная» терапия ИКВС должна проводиться препаратами, обладающими вазоактивными, нейропротективными и метаболическими свойствами (кавинтон, вазобрал, пирацетам, мексикор). Чрезвычайно важным является то, что данная терапия направлена на коррекцию локальных патофизиологических механизмов — нарушенного тонуса мозговых артерий и вен, метаболических процессов в мозге, гемореологии и микроциркуляции [32]. Клинический эффект этих препаратов обычно достигается в течение 10—14 дней. Продолжительность курса лечения и выбор препарата определяются врачом индивидуально. Вследствие снижения тонуса мозговых вен и нарушений венозного оттока с успехом применяют венотоники (троксевазин, танакан). В связи с тем, что особую роль в клинической и морфологической картинах ишемии играет оксидантный стресс, используются препараты, обладающие нейрометаболическими эффектами, которые улучшают выживаемость нейронов в условиях хронической гипоксии. Некоторые из них обладают антиоксидантными свойствами.
Одним из наиболее известных, детально изученных лекарственных препаратов в этой области является этилаповинкаминат (кавинтон, ОАО «Гедеон Рихтер») [8]. Кавинтон — этиловый эфир аповинкаминовой кислоты, синтетическое производное винкамина, естественного алкалоида барвинка малого. Механизм действия препарата складывается из ингибирования фосфодиэстеразы (Са/кальмодулинзависимой 1-го типа), приводящего к повышению уровня цАМФ и цГМФ и ингибированию потенциалзависимых Na+-каналов — защита от избыточной нейрональной активации. Кавинтон оказывает непосредственное воздействие на глютаматные рецепторы, ингибирует перекисное окисление липидов за счет нормализации клеточных процессов, захват аденозина, вызывает вазодилятацию, повышает внутриклеточный уровень цГМФ в гладкой мускулатуре сосудистой стенки, причем по степени выраженности данного эффекта значительно превосходит все вазодилататоры, тормозит агрегацию тромбоцитов, увеличивает деформацию эритроцитов. Сочетание выраженного снижения сопротивления церебральных артерий и практически стабильного уровня системного давления позволяет расценивать вазодилатирующий эффект кавинтона как избирательный в отношении мозговых артерий. У пациентов со стабильно повышенным уровнем системного артериального давления применение кавинтона сопровождается умеренным гипотензивным эффектом (давление снижается на 10—15 мм рт.ст.).
В то же время установлено, что внутривенное введение препарата у пациентов с исходно нормальным или даже низким уровнем давления сопровождалось очень умеренным его повышением (не более чем на 20/10 мм рт.ст.). Он оказывает нормализующее действие на мозговые сосуды как с повышенным, так и с пониженным тонусом, препятствуя, в частности, неадекватным сосудистым реакциям. Препарат восстанавливает способность к ауторегуляции мозгового кровообращения, предотвращает развитие вазоконстрикторных изменений, обусловливающих феномен «no-reflow» в раннем постишемическом периоде. Препарат на 40% предотвращает потерю нейронов в области гиппокампа, обладает выраженным мембраностабилизирующим эффектом, стимулирует норадренергическую систему восходящей ретикулярной формации, участвует в модуляции пластичности (увеличивает рост дендритических шипиков). Терапевтический эффект при применении кавинтона наблюдается с первого дня лечения. Его выраженность увеличивается по мере приема препарата. Отсроченные эффекты сохраняются в течение 1 года после окончания терапии. Курсовая терапия кавинтоном улучшает общее клиническое состояние больных с ИКВС, их умственную и физическую работоспособность. Терапия новыми формами кавинтона (25 мг/5 мл и 50 мг/10 мл) и кавинтона форте (10 мг №90) по новой схеме значительно уменьшает субъективные проявления цереброваскулярных заболеваний: головную боль на 82%, головокружение на 75%, шум в ушах на 46%. Наиболее выраженная положительная динамика выявлена по регрессу глазодвигательных нарушений, нистагма, вестибуло-атаксического и амиостатического синдромов [8]. Улучшение когнитивных функций при лечении кавинтоном вызвано его корригирующим действием на различные звенья хронической гипоперфузии головного мозга. Эффективность и безопасность длительного использования препарата (1—2 года) подтверждены исследованиями, проведенными в Венгрии, Германии, Италии и Японии (категория доказательств В). Препарат используют в суточной дозе 25—50 мг внутривенно (капельно) в течение 7—10 дней, с последующим переходом на прием внутрь препарата кавинтон форте по 10 мг 3 раза в день в течение 1—3 мес.
Понимание механизма действия лекарственных веществ на организм расширяет диапазон возможностей медикаментозной терапии ТКВС. Эффективность лекарственного средства определяется с позиций доказательной медицины и выражается в уменьшении клинических проявлений заболевания и улучшении качества жизни больного. Особое место занимают вопросы безопасности применения лекарственных средств. Окончательное заключение о неэффективности выбранного лечения и необходимости его коррекции можно делать в случае отсутствия терапевтического эффекта после 2—3 курсов длительностью не менее 3 мес. Не следует отказываться от выбранного препарата, если его доза не была повышена до индивидуально максимальной и хорошо переносимой. В случае недостаточной эффективности, но хорошей переносимости лекарственного вещества к нему можно добавить второй препарат из другого класса. Современные знания дают возможность комбинированного назначения двух или нескольких лекарственных средств. Наиболее оптимальная комбинация — сочетание вертилолитического препарата (бетагистин) + нейропротектора (кавинтон) + энергокорректор (актовегин). Это сочетание может дать более выраженный лечебный эффект при меньшей вероятности возникновения побочных явлений, т.к. используются более низкие дозы. Однако должно соблюдаться следующее правило: раннее начало и длительное продолжение (до 3—4 мес) терапии.
Таким образом, ИКВС, имея разные этиопатогенетические механизмы, требуют тщательной диагностики, ранней комплексной медикаментозной терапии и последующей нейрореабилитации.
2.Причины
Кохлеарные невриты могут развиваться под действием множества факторов:
- инфекционные болезни (грипп, корь, ОРВИ, герпес, скарлатина и т.д.);
- интоксикации солями тяжелых металлов, промышленными углеводородами, лекарственными средствами (антибиотики, химиотерапия, антиаритмики, мочегонные и пр.);
- производственные вредности (вибрация, зашумленность);
- острые и хронические состояния, связанные с нарушениями цереброваскуляции (кровоснабжения головного мозга);
- черепно-мозговые, акустические, лучевые, родовые травмы;
- онкозаболевания;
- нейродегенеративные процессы и возрастные изменения.
Как видно из перечисленного, в большинстве случаев кохлеарный неврит носит приобретенный характер. Встречается, однако, и врожденная нейросенсорная тугоухость, обусловленная, как правило, наследственными факторами и выступающая одним из элементов того или иного хромосомного синдрома.
Посетите нашу страницу Отоларингология (ЛОР)
Диагностика
Диагностика синдрома вертебральной артерии представляет определенные сложности и Нередко происходит как гипердиагностика, так и гиподиагностика синдрома вертебральной артерии. Гипердиагностика синдрома часто обусловлена недостаточным обследованием пациентов особенно при наличии вестибуло-атактического и/или кохлеарного синдрома, когда врачу не удается диагностировать заболевания лабиринта.
Для установления диагноза синдрома позвоночной артерии необходимо наличие 3 критериев.
- Наличие в клинике симптомов одного из 9 клинических вариантов или сочетание вариантов
- Визуализация морфологических изменений в шейном отделе позвоночника с помощью МРТ или МСКТ которые могут быть основными причинами развития этого синдрома.
- Наличие при УЗИ исследовании изменений кровотока при выполнении функциональных проб со сгибанием – разгибанием головы ротацией головы.
3.Симптомы и диагностика
Наиболее типичными проявлениями кохлеарного неврита, помимо собственно тугоухости, являются ощущения постоянного постороннего шума в голове и асимметричность снижения слуха. У некоторых больных отмечается также комплекс вестибулярных нарушений (головокружения, расстройства координации и равновесия, шаткость походки и т.п.).
Очевидно, что любая тугоухость, в т.ч. обусловленная кохлеарным невритом, является социально-значимой проблемой, поскольку приводит к нарушениям коммуникации и социального функционирования, требует применения слуховых аппаратов, во многих случаях ограничивает или исключает профессиональную пригодность, провоцирует развитие психологических расстройств депрессивного регистра.
Степень функциональной несостоятельности слухового анализатора устанавливается в серии аудиометрических, камертональных и других подобных проб. Производится отоскопия, микроотоскопия; назначаются также электрокохлеаграфия, вестибулометрические исследования, консультации (и соответствующие обследования) профильных специалистов, батарея лабораторных тестов.
О нашей клинике м. Чистые пруды Страница Мединтерком!
Симптомы
По клиническому течению различают две стадии синдрома вертебральной артерии функциональную и органическую.
Для функциональной стадии синдрома вертебральной артерии характерна определенная группа симптомов: головные боли с некоторыми вегетативными нарушениями кохлеовестибулярные и зрительные нарушения. Головная боль может иметь различные формы, как острая пульсирующая, так и ноющая постоянная или резко усиливающаяся особенно при поворотах головы или длительных статической нагрузке. Головная боль может распространяться от затылка ко лбу. Нарушения в кохлеовестибулярной системе могут проявляться головокружением пароксизмального характера (неустойчивость покачивание) или системного головокружения. Кроме того, возможно некоторое снижение слуха. Нарушения зрительного плана могут проявляться потемнением в глазах, ощущением искр, песка в глазах.
Длительные и продолжительные эпизоды сосудистых нарушений приводят к формированию стойких очагов ишемии в головном мозге и развитию второй (органической) стадии синдрома вертебральной артерии. В органической стадии синдрома появляются симптомы как транзиторных, так и стойких гемодинамических нарушений головного мозга. Транзиторные гемодинамические нарушения проявляются такими симптомами, как головокружение, тошнота, рвота, дизартрия. Кроме того, существуют и характерные формы ишемических атак, которые возникают во время поворота или наклона головы, при которых могут возникать приступы падения с сохраненным сознанием, так называемые дроп — атаки, а также приступы с потерей сознания длительностью до 10 минут (синкопальные эпизоды). Симптоматика, как правило, регрессирует в горизонтальном положении и как считается, обусловлена транзиторной ишемией ствола головного мозга. После таких эпизодов могут наблюдаться общая слабость шум в ушах вегетативные нарушения.
По типу гемодинамических нарушений различают несколько вариантов синдрома позвоночной артерии (компрессионная, ирритативная, ангиоспатическая и смешанная формы).
Сужение сосуда при компрессионном варианте происходит вследствие механической компрессии на стенку артерии. При ирритативном типе синдром развивается вследствие рефлекторного спазмам сосуда из-за ирритации симпатических волокон. В клинике, чаще всего, встречаются комбинированные (компрессионно-ирритативные) варианты синдрома позвоночной артерии. При ангиоспастическом варианте синдрома также имеется рефлекторный механизм, но возникает от раздражения рецепторов в области двигательных сегментов шейного отдела позвоночника. При ангиоспастическим варианте преобладают вегето-сосудистые нарушения и симптоматика не так сильно обусловлена с поворотами головы.
4.Лечение
Эффективная этиотропная терапия возможна лишь в тех случаях, когда идентифицированы причины поражения нерва и когда эти причины носят обратимый характер. В разных ситуациях назначается неврологическое, антибиотическое, противовирусное, физиотерапевтическое лечение (роль и возможности последнего весьма велики и до настоящего времени исследованы недостаточно). В некоторых случаях слух восстанавливается после хирургической операции, устраняющей, например, фактор механического давления на нерв.
Согласно публикуемым сегодня данным, значительного улучшения или полного восстановления слуховой функции удается добиться примерно в 80% случаев. При неэффективности всех принимаемых мер подбирается слуховой аппарат; характеристики и дизайн современных высокотехнологичных цифровых моделей позволяют кардинально снизить психологические, социальные и профессиональные ограничения, обусловленные тугоухостью.