ВИЧ-инфекция — прогрессирующее антропонозное заболевание с преимущественно контактным механизмом заражения, характеризующееся специфическим поражением иммунной системы с развитием иммунодефицита, который проявляется развитием оппортунистических инфекций, злокачественных новообразований, возникновением аутоиммунных реакций.
За период с момента начала изучения ВИЧ-инфекции в мире зарегистрировано более 60 млн человек с ВИЧ. Особенно острой эта проблема является для России и стран СНГ, где заболеваемость ВИЧ выше, чем в других регионах мира [1]. В России более 700 тыс. больных, при этом оценочные показатели превосходят реальную выявляемость в 2—4 раза [2, 3].
Вследствие внедрения в клиническую практику высокоактивной антиретровирусной терапии (ВААРТ) ВИЧ-инфекция перешла из категории смертельных заболеваний в хроническое, медикаментозно регулируемое заболевание с ожидаемой продолжительностью жизни человека в несколько десятилетий. Тем не менее масштабы распространенности заболевания остаются пока высокими.
ВИЧ имеет большое генетическое разнообразие, формируя типы, группы, подгруппы и рекомбинантные формы, которые могут (помимо общих свойств) в силу генетических различий приобретать биологические особенности, в том числе тропность к поражению ЦНС, что в последние годы является предметом активного обсуждения [4]. По частоте поражения различных органов и систем при ВИЧ-инфекции, вызывающей синдром приобретенного иммунодефицита (СПИД), нервная система (нейроСПИД) стоит на втором месте после иммунной. Это связано с множеством патогенетических механизмов поражения как центральной, так и периферической нервной системы [5]. По данным аутопсий, патоморфологические изменения нервной системы встречаются у 70—80% умерших от СПИДа. Поражение ЦНС при ВИЧ-инфекции является, как правило, важным инвалидизирующим фактором. У 40—60% пациентов имеются разнообразные неврологические, психические и когнитивные нарушения, что значительно затрудняет их социальную адаптацию, а в тяжелых случаях приводит к полной инвалидизации.
Неврологические проявления ВИЧ-инфекции могут быть вызваны как самим ВИЧ, так и оппортунистическими инфекциями, новообразованиями, а также токсическим воздействием антиретровирусных препаратов. Непосредственное действие ВИЧ на клетки нервной системы заключается в инфицировании и разрушении клеток, имеющих рецептор CD4 (клетки микроглии, астро-, моно-, олигодендроциты, клетки эндотелия кровеносных сосудов и сами нейроны) [6]. Кроме того, клетки ЦНС разрушаются мембранным белком gp 120, который играет ключевую роль в патогенезе нейрональных повреждений за счет блокирования нейролейкина. Различные патогенетические механизмы способны приводить к возникновению клинических проявлений с разнообразным неврологическим дефицитом [7].
В патогенезе неврологических расстройств важную роль играют сложные биохимические нарушения. Изменение регуляторной активности гипоталамо-гипофизарной системы ведет к нарушениям нейромедиаторного обмена, дефициту γ-аминомасляной кислоты и глицина, которые ассоциированы с развитием эпилептических приступов, уменьшение выработки серотонина — к возникновению депрессивных расстройств и атаксии, нарушение обмена вазопрессина — к расстройствам памяти, поражение эндотелиальных клеток сосудистых сплетений оболочек мозга и эпендимы желудочков — к развитию вторичной демиелинизации; депрессия клеточного иммунитета — к развитию оппортунистических инфекций и неопластических процессов. Как правило, имеет место сочетание указанных факторов, что определяет клинические проявления поражения ЦНС у конкретного больного.
В настоящее время выделяют ряд первичных и вторичных поражений ЦНС при ВИЧ-инфекции:
— синдром приобретенного иммунного дефицита, сочетающий проявления инфекционного и дегенеративного процессов (нейроСПИД);
— синдром СПИД-деменции;
— ВИЧ-ассоциированные нейрокогнитивные нарушения (HIV-associated neurocognitive disorders — HAND);
— ВИЧ-ассоциированная энцефалопатия;
— ВИЧ-обусловленные поражения ЦНС (первичные);
— оппортунистические поражения ЦНС [1].
К первичным поражениям нервной системы при ВИЧ относят нарушения, связанные с непосредственным влиянием вируса: НAND, ВИЧ-ассоциированные энцефало-, миело-, полинейропатии, другие поражения ЦНС, обусловленные ВИЧ-инфекцией (асептический менингит, менингоэнцефалит). HAND является клиническим диагнозом у ВИЧ-инфицированных пациентов, имеющих когнитивные расстройства, в случае если на основании клинических и лабораторных исследований исключены инфекционные и метаболические поражения ЦНС, депрессия и другие причины. Установление диагноза требует целостной оценки вирусологического и иммунного статуса больного, оценки характера принимаемых им препаратов, употребления наркотических средств, анализа сопутствующих заболеваний, а также невро- и психоневрологического обследования. Обычно HAND не связаны с нарушением уровня сознания, очаговой неврологической симптоматикой либо признаками системного поражения.
ВИЧ-ассоциированные мягкие познавательно-двигательные расстройства
встречаются более чем у 80% больных СПИДом [8]. Проведенное на начальных стадиях заболевания неврологическое обследование может не выявить никаких отклонений, однако при нейропсихологическом тестировании, как правило, выявляются нарушения выполнения нейропсихологических тестов, соответствующие умеренным или более выраженным когнитивным нарушениям. При осмотре могут выявляться признаки диффузного симметричного поражения пирамидных путей, гиперрефлексия и симптомы поражения лобных долей. Выявляемые расстройства включают моторную и психомоторную заторможенность, нарушение внимания, неспособность сосредоточиться, мнестические нарушения, затруднения в обучении, обработке информации [9]. На ранних стадиях заболевания страдает кратковременная память, что связано с нарушением запоминания и извлечения информации.
ВИЧ-энцефалопатия (комплекс СПИД — деменция), как правило, развивается на поздних стадиях ВИЧ-инфекции и имеет различную выраженность симптоматики вплоть до развития деменции. Синдромологически представляет собой подкорковую деменцию, которая обычно развивается в течение нескольких недель или месяцев. Острое развитие нейропсихологической симптоматики указывает на другую причину энцефалопатии. Часто первые проявления энцефалопатии вначале замечают близкие больного, а не он сам. Характерными являются замедленность мышления, забывчивость, затруднение концентрации внимания, ощущение упадка сил, проявления депрессии, притупление эмоций, затруднение при выполнении тонких движений (например, при письме, застегивании пуговиц), появление императивных позывов к мочеиспусканию, эректильная дисфункция.
Можно выделить несколько групп симптомов ВИЧ-энцефалопатии:
1. Неврологические: на ранней стадии они могут отсутствовать или иметь незначительную выраженность. Возможны нарушение походки, замедление выполнения быстро чередующихся движений, гипомимия, тремор. В последующем отмечаются повышение рефлексов, появление патологических рефлексов, замедление саккадических движений глазных яблок, тазовые нарушения, возможно развитие сопутствующей полинейропатии. Для терминальной стадии характерно развитие спастической тетраплегии и недержание мочи и кала. 2. Когнитивные нарушения с замедлением психомоторной деятельности, расстройствами кратковременной памяти и переключения внимания. Динамика психических нарушений также носит стадийный характер. На ранней стадии заболевания выявляются повышенная отвлекаемость, притупление эмоций, сглаженность личностных черт, безынициативность. На поздних стадиях больной может быть дезориентирован во времени, пространстве и ситуации. В итоге, как правило, развивается мутизм.
Нарушения сознания, менингеальные симптомы, очаговая неврологическая симптоматика для ВИЧ-энцефалопатии не характерны. Психотические расстройства (без когнитивных или двигательных нарушений) также не соответствуют диагнозу ВИЧ-энцефалопатии. Редко такая энцефалопатия проявляется и парциальными или генерализованными судорожными приступами.
Диагноз большей частью ставится методом исключения. Когнитивные и психические нарушения всегда сочетаются с двигательными, хотя последние могут быть слабо выражены. Для выявления и оценки тяжести когнитивных нарушений при ВИЧ-энцефалопатии удобно пользоваться соответствующими психометрическими полуколичественными шкалами [10].
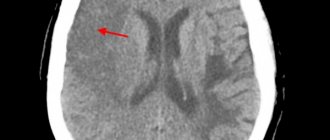
Лабораторные и инструментальные исследования направлены в основном на исключение других причин неврологических нарушений. Из методов нейровизуализации предпочтительнее использовать МРТ, при проведении которой выявляются признаки лейкоэнцефалопатии (относительно симметричное очаговое и диффузное изменение плотности белого вещества головного мозга), никогда не распространяющиеся на корковые отделы. Иногда наблюдается атрофия вещества мозга с расширением желудочков и борозд полушарий головного мозга. Отек вещества головного мозга, сдавление тканей и усиление МР-сигнала при контрастном усилении не характерны для ВИЧ-энцефалопатии и должны наводить на мысль о каком-либо другом процессе, вместе с тем возможно слабо выраженное симметричное диффузное контрастное усиление МР-сигнала от базальных ганглиев. Указанные изменения не носят специфического характера. Иногда изменения при МРТ отсутствуют. На ЭЭГ очаговые изменения отсутствуют, иногда обнаруживаются легкие признаки диффузного замедления биоэлектрической активности.
Изменения в цереброспинальной жидкости (ЦСЖ) неспецифичны. У пациентов, получающих высоактивную антиретровирусную терапию (ВААРТ), в ЦСЖ может обнаруживаться плеоцитоз, свидетельствующий об иммунологическом ответе на ВИЧ на фоне восстановления иммунной системы. Еще до широкого внедрения в клиническую практику ВААРТ была установлена слабая, но статистически значимая связь между высокой вирусной нагрузкой в ЦСЖ и выраженностью проявлений ВИЧ-энцефалопатии.
Лечение ВИЧ-энцефалопатии должно быть направлено на подавление репликации ВИЧ в ЦНС, поэтому основным направлением терапии является назначение антиретровирусных препаратов. Предпочтение должно отдаваться лекарственным средствам, хорошо проникающим через гематоэнцефалический барьер. ВААРТ привела к сокращению частоты случаев ВИЧ-энцефалопатии в 2 раза [11, 12], при этом продолжительность жизни увеличилась с 6 до 48 мес и более. Количество клеток СD4 в периферической крови на фоне лечения увеличивается с 50—100 в 1 мкл до нормального уровня [13]. На фоне ВААРТ может наблюдаться существенное клиническое улучшение течения ВИЧ-энцефалопатии, даже восстановление трудоспособности у пациентов, которые ранее нуждались в постороннем уходе. В течение первых месяцев лечения, несмотря на значительное клиническое улучшение, нейровизуализационные признаки лейкоэнцефалопатии могут нарастать, однако в течение последующих 1—2 лет постепенно исчезают. В настоящее время считается, что наличие даже минимальных когнитивных нарушений является достаточным основанием для назначения ВААРТ [14]. Дополнительное назначение ноотропных, нейрометаболических средств носит вспомогательный характер, поскольку не способно снизить репликацию вируса, однако может способствовать замедлению вызванных им нейродегенеративных процессов.
Острый ВИЧ-ассоциированный менингоэнцефалит
представляет собой наиболее тяжелую острую редко возникающую форму первичного поражения ЦНС при ВИЧ-инфекции. Острый энцефалит связывается с прямым поражением клеток головного мозга вирусом иммунодефицита человека. Развитие ВИЧ-менингоэнцефалита совпадает по времени или даже предшествует изменению результатов серологических исследований. В дебюте заболевания возможны угнетение сознания (вплоть до коматозного), эпилептические приступы. Неврологическая симптоматика в течение нескольких недель может полностью регрессировать, однако в дальнейшем у части больных, перенесших острый менингоэнцефалит, возможно развитие хронической ВИЧ-энцефалопатии. При соматическом обследовании могут выявляться генерализованная лимфоаденопатия, спленомегалия, макулопапулезная сыпь, крапивница. В ЦСЖ определяются неспецифические воспалительные изменения в виде плеоцитоза; нейровизуализационные признаки поражения мозга могут отсутствовать.
В острой стадии дифференциальный диагноз проводится с энцефалитом, вызванным вирусом простого герпеса. Последний может быть исключен, если в течение 3 дней при повторном КТ-сканировании не будет выявлено патологии мозга в виде очагов пониженной плотности.
Широкое применение ВААРТ привело к увеличению продолжительности течения заболевания и сделало его более благоприятным — чаще наблюдаются хронические формы менингоэнцефалита, чем острые и подострые [15].
У 20% ВИЧ-инфицированных пациентов чаще при тяжелом иммунодефиците развивается ВИЧ-ассоциированная миелопатия.
Она может развиваться без сопутствующих когнитивных и психических нарушений, свойственных ВИЧ-энцефалопатии. В клинической картине преобладают нарушения походки вследствие повышения мышечного тонуса по спастическому типу и атаксии конечностей, гиперрефлексия, патологические рефлексы, тазовые нарушения, в частности эректильная дисфункция. Чувствительность может быть нарушена по проводниковому типу или типу «носков» и «перчаток» вследствие сопутствующей полинейропатии. Изолированная ВИЧ-миелопатия может диагностироваться в случаях, когда сопутствующие когнитивные нарушения выражены менее, чем симптомы миелопатии, или отсутствуют. В диагностике основная роль отводится методам нейровизуализации и электрофизиологическим исследованиям, выявляется увеличение латентного периода соматосенсорных и двигательных вызванных потенциалов при транскраниальной магнитной стимуляции. Лечение основано на проведении ВААРТ.
У ВИЧ-инфицированных пациентов на любой стадии ВИЧ-инфекции возможно развитие синдромов поражения периферической нервной системы, которые наблюдаются примерно у ½ пациентов. Наиболее часто в клинике встречаются полинейро- и полирадикулопатии, которые могут развиваться вследствие как непосредственного действия ВИЧ, так и оппортунистических инфекций.
Наиболее часто развивается дистальная симметричная сенсорная полинейропатия
. Возникает она, как правило, на поздних стадиях ВИЧ-инфекции, когда количество лимфоцитов CD4 становится менее 200 в мкл. Риск ее развития выше у пациентов старшего возраста, а также употребляющих наркотические препараты [16]. Менее убедительна связь поражения периферических нервов с приемом применения нейротоксичных противовирусных препаратов. Заболевание проявляется медленно нарастающими нарушениями чувствительности — ощущениями онемения, покалывания, ползания мурашек на стопах и голенях. Примерно у 30—50% больных развивается нейропатический болевой синдром с возникновением жгучих, режущих или колющих болей в дистальных отделах конечностей. При осмотре выявляются снижение или отсутствие ахилловых рефлексов, повышение порога вибрационной чувствительности на пальцах ног, стопах, лодыжках и снижение болевой чувствительности в дистальных отделах конечностей, проприоцептивная чувствительность, как правило, не нарушается. Слабость и атрофия мышц стопы выражены незначительно. Кисти и пальцы рук поражаются редко. У многих больных с дистальной симметричной сенсорной полинейропатией утрата или нарушение функции малых симпатических и парасимпатических нервных волокон может вызвать ортостатическую гипотензию, эректильную дисфункцию. В диагностике используется электонейромиография, при которой выявляется аксональный тип повреждения нервных волокон.
При ВИЧ-инфекции встречаются также острая и хроническая воспалительная демиелинизирующая полинейропатия (ОВДП и ХВДП)
. ОВДП обычно развивается во время сероконверсии или на бессимптомной стадии ВИЧ-инфекции, редко может возникать на фоне восстановления иммунной системы. Протекает по типу синдрома Гийена—Барре. В ЦСЖ у ВИЧ-инфицированных пациентов (в отличие от ВИЧ-негативных) часто обнаруживается умеренный плеоцитоз. Примерно у 1/3 больных наблюдаются остаточные явления разной степени тяжести.
ХВДП — хроническое прогрессирующее и рецидивирующее заболевание, характеризующееся развитием в течение нескольких месяцев вялых парезов и невритических нарушений чувствительности. В некоторых случаях рецидивы чередуются с неполными ремиссиями и периодами стабилизации. При ХВДП, как и ОВДП, в ЦСЖ повышается уровень белка, часто обнаруживается умеренный плеоцитоз. ХВДП является редким осложнением ВИЧ-инфекции и развивается, как правило, вскоре после сероконверсии или на ранних стадиях ВИЧ-инфекции.
Важное место среди вторичных поражений нервной системы при ВИЧ-инфекции занимают токсические лекарственные нейропатии
, связанные с назначением антиретровирусных, антимикробных, цитостатических препаратов. Примерно у 10—30% больных, получающих диданозин, ставудин или зальцитабин, развивается дистальная симметричная сенсорная полинейропатия, которая клинически и электрофизиологически неотличима от полинейропатии, обусловленной ВИЧ-инфекцией. Единственное отличие — прием нейротоксических нуклеозидных ингибиторов обратной транскриптазы (НИОТ) в анамнезе. Нуклеозидная нейропатия развивается в среднем через 12—24 мес от начала приема препарата. После его отмены состояние иногда продолжает ухудшаться в течение 2—4 нед, но через 1,5—3 мес обычно начинается улучшение. Иногда восстановление бывает неполным из-за исходного поражения периферических нервных волокон, обусловленного ВИЧ-нейропатией. При субклиническом нарушении функции периферических нервов, подтвержденном результатами электронейрографии, риск развития нейропатии на фоне приема НИОТ возрастает.
Полинейро- и полирадикулопатии на поздних стадиях ВИЧ-инфекции могут быть осложнением оппортунистических заболеваний. Множественная мононейропатия в большинстве случаев является осложнением цитомегаловирусной инфекции (ЦМВ) и неходжкинской лимфомы. Острая и подострая полирадикулопатия, в частности синдром конского хвоста с быстро прогрессирующим вялым нижним парапарезом, недержанием кала и нарушениями чувствительности, может быть обусловлена оппортунистическими инфекциями, а также опухолевой инфильтрацией мозговых оболочек при лимфоме. Другими причинами полинейропатий являются хронический алкоголизм, сахарный диабет, истощение при хронических заболеваниях желудочно-кишечного тракта, новообразования.
Диагностика нейропатий при ВИЧ-инфекции обычно основана на данных анамнеза, клинического осмотра. Для подтверждения диагноза и исключения других заболеваний необходимо проведение электронейрографии. При подозрении на оппортунистические инфекции обязательно проводится исследование ЦСЖ. Биопсия икроножного нерва и мышцы требуется только в атипичных случаях, например при болевой дистальной симметричной сенсорной понинейропатии у пациента с высоким количеством клеток CD4 и низкой вирусной нагрузкой, который не принимает нейротоксические препараты, и при отсутствии других факторов риска. Иногда при наличии жалоб пациента объективное обследование, в том числе электрофизиологическое, не выявляет никаких изменений. В этом случае симптомы могут быть обусловлены изолированной нейропатией мелких немиелинизированных вегетативных нервных волокон. Для уточнения диагноза требуются пункционная биопсия периферического нерва с гистологической оценкой плотности внутриэпидермальных нервных волокон или регистрация связанных с болью соматосенсорных вызванных потенциалов.
Основными причинами вторичных поражений ЦНС при ВИЧ-инфекции являются оппортунистические инфекции и новообразования, которые развиваются на поздних стадиях ВИЧ-инфекции, в стадии СПИДа. Многие из них часто приводят к смерти больного. Токсоплазмоз — наиболее частая причина очагового поражения ЦНС у больных СПИДом (выявляется приблизительно у 10% больных). В большинстве случаев является результатом реактивации латентной инфекции. Методы нейровизуализации играют решающую роль в диагностике токсоплазмоза. При нейровизуализации выявляются области поражения вещества головного мозга с отеком, более интенсивным окрашиванием при внутривенном контрастировании, чаще в виде колец. Очаги поражения обычно обнаруживаются в базальных ганглиях. Токсоплазмоз ЦНС у больных СПИДом часто рецидивирует после прекращения лечения, поэтому большинство больных нуждаются в постоянной поддерживающей терапии [17, 18].
Первичная лимфома ЦНС выявляется у 5% больных СПИДом. Неврологические симптомы могут указывать на очаговое или диффузное поражение ЦНС. У таких больных имеется высокий титр антител к вирусу Эпштейна—Барр. При использовании методов нейровизуализации выявляются один (или более) гипер- или изоденсивный очаг с признаками отека вещества мозга, однако изменения не являются специфичными для лимфомы [19].
К герпесвирусным осложнениям СПИДа относят поражение ЦНС цитомегаловирусом, вирусами Herpes
zoster
, простого герпеса 1-го и 2-го типа. Они могут быть причиной поражения как вещества головного мозга, так и его оболочек. Опоясывающий лишай обычно является следствием реактивации латентной инфекции и встречается на разных этапах ВИЧ-инфекции. Больные СПИДом чаще имеют диссеминированный герпес и постгерпетический неврологический синдром, а также многоочаговые лейкоэнцефалиты с очаговой или латерализованной неврологической симптоматикой и признаками гидроцефалии [20].
Также часто к инфекционному поражению головного мозга и его оболочек у больных СПИДом приводят туберкулез, сифилис, грибковая инфекция. Инфекционные поражения ЦНС, как правило, наблюдаются у пациентов с поздними стадиями СПИДа [21]. Диагностика этих заболеваний обусловлена особенностями каждого из них, но инфекция часто верифицируется только ретроспективно, в частности при ответе на специфическую терапию. Подозрение может возникать при анализе клинической симптоматики, данных нейровизуализационного обследования, реже — при проведении серологических исследований или по данным биопсии. Часто имеется сочетанная инфекция несколькими возбудителями.
Таким образом, неврологические нарушения при ВИЧ-инфекции очень разнообразны, в ряде случаев именно они являются первыми симптомами ВИЧ-инфекции и могут послужить поводом для назначения ВААРТ.
Что такое ВИЧ-энцефалопатия?
ВИЧ — это вирус, который поражает и ослабляет иммунную систему, что может увеличить риск и последствия потенциальных осложнений. Одним из таких осложнений является ВИЧ-энцефалопатия. Обычно это происходит из-за воздействия на мозг вируса или оппортунистических инфекций, таких как токсоплазмоз.
ВИЧ-энцефалопатия обычно появляется, когда ВИЧ достигает последних стадии, поэтому может проявляться через много лет после инфицирования. Это состояние чаще встречается у людей, которые не принимают эффективные препараты от ВИЧ, и тех, у кого очень низкое количество CD4-клеток, являющихся типом белых кровяных клеток, которые борются с инфекциями. ВИЧ-энцефалопатия встречается реже у людей, которые проходят раннее и непрерывное лечение.
ВИЧ-энцефалопатия — диагностика
Диагностика ВИЧ-энцефалопатии затруднена, поскольку многие факторы могут способствовать появлению симптомов. К ним относятся:
- дефицит питательных веществ
- депрессия
- побочные эффекты медикаментозных препаратов
- оппортунистические инфекции
При постановке диагноза врачи могут использовать следующие диагностические тесты:
- тесты психического статуса
- нейропсихологическое тестирование
- основные тесты физических способностей или движений
- МРТ-сканирование
- компьютерная томография
- анализы крови
- анализы спинномозговой жидкости
Лечение ВИЧ-энцефалопатии
Без лечения ВИЧ-энцефалопатия может привести к летальному исходу. Данные свидетельствуют, что ни одно специфическое лечение не способно вылечить все осложнения ВИЧ-энцефалопатии. Людям могут потребоваться различные препараты, такие как опиоиды, противосудорожные препараты, антидепрессанты и антиретровирусная терапия, для лечения различных симптомов.
Антиретровирусная терапия является основным методом лечения ВИЧ. Это комбинация препаратов, которая уменьшает количество вируса в крови. Исследования показывают, что лекарственные средства могут обратить вспять некоторые повреждения, возникающие в результате ВИЧ-энцефалопатии, что потенциально может повысить баллы по тестам, которые анализируют навыки мышления.
В статье, опубликованной в 2021 году, антиретровирусная терапия описывается как наиболее эффективное лечение ВИЧ-энцефалопатии, отмечая, что лечение снижает распространенность тяжелых случаев. Эффекты лечения:
- обращение вспять некоторых повреждений мозга от ВИЧ
- улучшение результатов нейропсихологических и когнитивных тестов
- отсрочка появления симптомов, указывающих на повреждение головного мозга
Однако эффективность антиретровирусной терапии при более легких формах когнитивного снижения, связанного с ВИЧ, неясна. Отсутствие доказательств связано с тем фактом, что когнитивные трудности в таких случаях незначительны, поэтому они иногда остаются не диагностированными.
ВИЧ-энцефалопатия — причины
Исследователи до сих пор точно не понимают механизм, который вызывает развитие ВИЧ-энцефалопатии. Однако большинство доказательств свидетельствуют о том, что это связано с воспалением и повреждением, которое возникают, когда вирус проходит через гематоэнцефалический барьер и поражает мозг. Некоторые данные также свидетельствуют, что ВИЧ может мутировать в головном мозге, что делает его отличным от вируса, циркулирующего в остальной части тела. Это может привести к тому, что некоторые методы лечения будут менее эффективными.
ВИЧ-энцефалопатия по стадиям
Всемирная организация здравоохранения (ВОЗ) перечисляет ВИЧ-энцефалопатию как симптом последней стадии ВИЧ.
Кроме того, это самая тяжелая из трех стадии ВИЧ-ассоциированного нейрокогнитивного расстройства:
- Бессимптомные нейрокогнитивные нарушения
: эта форма не имеет симптомов когнитивного снижения. - Легкое нейрокогнитивное расстройство, связанное с ВИЧ
: могут наблюдаться легкие симптомы когнитивного расстройства. - ВИЧ-энцефалопатия
: проявляется тяжелыми симптомами когнитивного снижения.