Нервно-мышечные заболевания
Это группа наследственных заболеваний, которые передаются на генетическом уровне (Х сцепленные, аутосомно-доминантные, аутосомно–рецессивные формы, формы наследуемые по материнской линии-митохондриальные). Около трети случаев заболеваний является результатом новых мутаций. С учетом структурной организации выделяют следующие уровни поражения нервно-мышечной системы:
- Первично-мышечные поражения (мышечная дистрофия Дюшена, Беккера, миопатии, миотонии).
- Синаптические поражения (нарушения нервно-мышечной передачи- миастении).
- Нейрональные поражения (спинальная мышечная атрофия).
МИОЗИТ
Миозит – это группа заболеваний, которые проявляются воспалениями в мышечных тканях. Вызывается миозит различными причинами, от которых зависит и прогноз болезни. Часто с такой проблемой сталкиваются люди с профессией, связанной с постоянным пребыванием в одной (часто неудобной физиологически) позе: водители, музыканты (скрипачи, пианисты), спортсмены (теннисисты), программисты и так далее.
Частыми причинами могут быть:
1. Инфекции вирусной или бактериальной природы (грипп).
2. Аутоиммунные болезни (ревматоидный артрит, склеродермия, красная волчанка и т. д.).
3. Влияние токсических веществ (алкоголизм, наркомания).
4. Длительный прием некоторых лекарств.
Миозит – симптомы и лечение
Болезнь проявляется появлением ноющей или тупой боли в пораженных тканях. При движении или надавливании она усиливается. Часто отмечается слабость мускулатуры. Покраснения и отечность кожи встречаются редко. Наиболее распространенные – шейный и поясничный миозиты. Развиваются из-за постоянного пребывания в неудобной позе, вследствие переохлаждения, перенесенных заболеваний. Часто боль отдается в другие зоны, усиливается при активности. Лечение направлено на подавление воспалений, ведение здорового образа жизни, применение дозированной физической активности.
СИМПТОМЫ НЕРВНО-МЫШЕЧНЫХ ЗАБОЛЕВАНИЙ
Основной признак нервно-мышечных заболеваний – это слабость мускулатуры. Клиническая картина зависит от области поражения (плечевой пояс, бедра, таз, нижние конечности, мышцы лица, дыхательная мускулатура).В зависимости от формы заболевания за мышечной слабостью и повышенной утомляемостью при физических нагрузках развиваются мышечные атрофии / псевдогипертрофии, появляются фасцикуляции, угнетаются сухожильные рефлексы, нарушается походка, появляются особые двигательные приемы при вставании из положения лежа и сидя. Нервно-мышечные заболевания протекают по стадиям. Определить этап развития патологических процессов поможет врач невролог при помощи медицинской диагностики.
Приобретенные заболевания мышц
Приобретенные заболевания мышц могут быть воспалительного, инфекционного, лекарственного, токсического генеза.
Воспалительные заболевания мышцы человека – полимиозит, дерматополимиозит, миозит с включениями, саркоидная миопатия.
Инфекционные миозиты могут быть вирусными, бактериальными, паразитарными и др. Основные симптомы – слабость в мышцах и боли – появляются остро. Иногда могут сопровождаться поражением кожи (дерматополимиозит). Отличительной особенностью течения данных заболеваний является повышение температуры тела.
ДИАГНОСТИКА
Диагностическая задача состоит в установлении уровня поражения нервно-мышечного аппарата, установить причину и определить есть ли специфическое лечение.
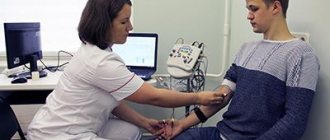
- Электронейромиография и электромиография. Диагностические методы помогают определить первичную и вторичную миопатию. Оценить также степень поражения спинного мозга и периферических нервов.
- Лабораторные тесты. Обязательно сдается клинический и биохимический анализ крови, чтобы определить уровень электролитов, белка, лактата, КФК, АлАТ, АсАТ, миоглобина а также гормонов щитовидной железы.
- Мышечная биопсия с патоморфологическим исследованием мышечной ткани. Результаты диагностики помогают установить точный диагноз (миодистрофия Дюшена, Беккера), что важно для подбора правильной терапии.
- Молекулярно-генетическая диагностика — максимально информативный метод диагностики, который назначается при нервно-мышечных заболеваниях.
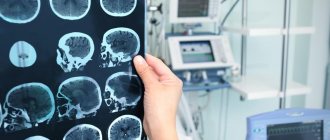
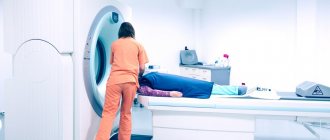
- Магнитно-резонансная томография головного мозга и шейного отдела позвоночника.
- Электрокардиограмма (ЭКГ) оценивает сердечный ритм.
- ЭХО КГ выявляет гипертрофическую, дилатационную кардиомиопатию.
ВИДЫ БОЛЕЗНЕЙ МЫШЦ
Мышечные заболевания подразделяются на группы, имеющие сходное возникновение, характерные проявления, течение и методы лечения.
К заболеваниям относят:
- миастении – слабость мышц вследствие аутоиммунных процессов;
- миалгии – болевые ощущения в мышечной ткани из–за спазма клеток;
- миозиты – воспалительные процессы, возникающие на фоне инфекций, заражений паразитами, других причин);
- рабдомиолиз – серьезное заболевание, развивающееся из-за разрушения скелетной мускулатуры и выброса миоглобина (белка) в кровь.
ЛЕЧЕНИЕ НЕРВНО-МЫШЕЧНЫХ ЗАБОЛЕВАНИЙ
Что касается лечения, то специфической терапии не существует. Терапевтический подход основывается на создании предпосылок к успешной реабилитации и обеспечении высокого качества общего и специализированного ухода.
- Медикаментозная терапия. Цель – компенсация энергетического дефицита мышечной ткани, улучшение тканевого метаболизма и периферического кровообращения. Применяются миотропные препараты, анаболические стероиды. В случае миодистофии Дюшена применяются глюкокортикостероиды. В случае миастении применяются антихолинэстеразные препараты. При вторичных повреждениях и / или дисфункции центральной нервной системы проводятся курсы нейропротективной и нейротрофической терапии. Медикаментозная терапия бульбарных, псевдобульбарных расстройств.
- Физиотерапия. Цель – коррекция метаболических нарушений, улучшение нервно-мышечной проводимости, нормализации мышечного тонуса, профилактика развития контрактур.
- Лечебная физкультура. Цель – предупреждение развития и коррекция контрактур конечностей, поддержание двигательной активности, улучшение мышечного тонуса, задержка развития атрофий, предупреждение осложнений, вызванных малоподвижностью. Обучение пациента пользоваться приспособлениями, позволяющими сидеть и стоять с поддержкой.
- Ортопедическая коррекция.
- Раннее выявление нарушения глотания (дисфагии) и возможности медикаментозной коррекции (совместно с ЛОР врачами, по результатам назофарингоскопии — функциональное состояние надгортанника, наличие регургитации, а у детей старшего возраста + анализ результатов рентген контрастного исследования акта глотания).
- Неврологическая оценка дыхательной функции (анализ ЭНМГ диафрагмальных нервов + УЗИ диафрагмы, анализ ФВД, пульсоксиметрии и капнометрии, механики и типе дыхания, данные ЭХО КГ, ЭКГ с заключением кардиолога).
Неврологическое обследование пациентов на предмет дыхательной недостаточности позволяет уточнить ее причины, обратимость нарушений и степень их компенсации. В случае сформировавшейся зависимости от искусственной вентиляции легких работа в команде врачей с созданием многофункциональной терапевтической программы, которая направлена на улучшение физического состояния и восстановление нормальных жизненных функций. выбор методов лечения и их очередности (медикаментозные и не медикаментозные, включая управление параметрами респираторной поддержки, дыхательную гимнастику, лечебную физкультуру, физиотерапевтические методики, психологическую помощь и прочее).
Среди наследственных заболеваний, затрагивающих мышечную и нервную системы, очень велика доля тех форм, которые могут сопровождаться интеллектуальным дефектом. При некоторых из этих заболеваний интеллектуальный дефект имеет врожденный непрогредиентный характер, при других — проявляется очень рано и медленно прогрессирует. Итак, наследственные
неврологические и нервно-мышечные заболевания должны встречаться и встречаются в контингенте умственно отсталых детей. Только среди врожденных или рано начавшихся атаксий и параплегии насчитывается не менее 40 генных дефектов, сопровождающихся умственной отсталостью [Калмыкова Л. Г., 1976]. Однако большинство из них встречается очень редко; многие описаны только в единичных семьях, часто у потомков родителей, находящихся в кровно-родственном браке.
По-нашему опыту, в контингенте умственно отсталых детей, обследованных в медико-генетической консультации, вся группа прогрессирующих заболеваний нервной и мышечной систем в целом составляет небольшую долю. Самые частые из них — миопатия Дюшенна и миотоническая дистрофия. Дети, страдающие этими заболеваниями, до развития выраженных проявлений со стороны мышечной системы нередко попадают под наблюдение детского психиатра с диагнозом «олигофрения».
Миотоническая дистрофия
(атрофическая миотония, дистрофическая миотония, болезнь Штейнерта — Баттона). Впервые заболевание было подробно описано в 1909 г. Его частота варьирует от 1:50 000 до 1:10 000. Необычно высокая распространенность миотонической дистрофии (1:3000) обнаружена в Северной Швеции.
Клиническая картина. Заболевание очень резко варьирует по клинической картине и срокам начала. При типичной картине оно начинается на 2—4-м десятилетии жизни и характеризуется развитием следующих симптомов: миотонии, атрофии мышц, особенно лица, шеи, дистальных отделов конечностей, катаракты, раннего облысения, атрофии гонад. Однако умственная отсталость встречается при внутриутробном начале этого заболевания.
Самый характерный симптом внутриутробного поражения — резко выраженный двусторонний парез лицевой мускулатуры, так называемая лицевая диплегия: лицо амимично, рот открыт, больной не может наморщить лоб, зажмурить глаза, улыбнуться. При этом родители нередко отмечают такое лицо у ребенка с первых недель жизни. Дети очень плохо сосут, не улыбаются. Для врожденной миотонической дистрофии характерна также общая мышечная гипотония. Мышцы мягкие, тестоватые на ощупь. Сухожильные рефлексы резко снижены или отсутствуют. Дыхание вследствие поражения дыхательной мускулатуры учащенное, поверхностное. Глотание часто затруднено, крик очень слабый. Нередко встречаются врожденные уродства — косолапость, гиперостозы и асимметрия черепа, артрогрипоз; небо всегда резко сужено, оно высокое, арковидное.
Дистрофические и особенно миотонические симптомы, характерные для заболевания при его обычном, позднем начале, у детей с внутриутробной формой болезни выявляются только в более старшем (дошкольном) возрасте, но и тогда в отличие от пораженных взрослых бывают выражены слабо. Катаракты (весьма частый симптом при позднем начале заболевания) у детей, как правило, не бывает.
У детей старшего возраста уже появляются и атрофические изменения в мышцах. Можно отметить и такие характерные для взрослых больных симптомы, как западения в области височных ямок вследствие атрофии мышц, легкая атрофия мышц голеней. Иногда отмечается своеобразный рост волос на лбу — залысины с обеих сторон. Миотонические симптомы у детей школьного возраста иногда уже легко выявляются при клиническом осмотре: дети медленно, с трудом разжимают сжатые в кулак пальцы при повторном действии.
Умственная отсталость при внутриутробном начале заболевания встречается у всех пораженных: IQ от 20 до 70 ед.
Вопрос о наличии прогредиентности в интеллектуальном снижении у детей является спорным. Истинная прогредиентность на клиническом уровне отсутствует. Более того, отмечается некоторая положительная динамика в развитии моторики и речи. Больным свойственны выраженная вялость, беспомощность даже при отсутствии заметных двигательных нарушений. Как правило, они робки и послушны.
Очень характерна тяжелая дизартрия вследствие изменений лицевой мускулатуры и мышц языка. При этом речь имеет выраженный носовой оттенок из-за фарингеального пареза.
Диагноз ставят на основании клинической картины; окончательно он может быть подтвержден в сомнительных случаях электромиографией, которая выявляет изменения, характерные для миотонии, а также молекулярной диагностикой мутантного гена.
Заболевание вызывается аутосомно-доминантным геном с резко варьирующей экспрессивностью. Мутантный ген передается практически всегда матерью. Наследование дефекта от матерей, возможно, связано с резкими эндокринными нарушениями у пораженных мужчин, приводящими к бесплодию. Механизм действия мутантного гена и патогенез умственной отсталости неясны. Но определены структура и локализация мутации. Заболевание вызывается (аналогично синдрому Мартина — Белл) амплификацией, т. е. повышением числа нуклеотидов в определенном регионе одной из хромосом (19ql3,3). Число повторов нуклеотидов увеличивается при передаче мутации из поколения в поколение. Тяжесть заболевания четко коррелирует с численностью этих повторов. Наибольшее их число определяется при врожденной тяжелой форме заболевания . Выявленный механизм объясняет феномен антиципации — утяжеления и все более раннего начала болезни в нисходящих поколениях.
Лечение. Специфического лечения не существует. При наличии атрофии применяют анаболические стероиды (ретаболил, неробол), общеукрепляющую терапию. В тех случаях, когда имеется значительно выраженная миотоническая симптоматика, назначают курсы дифенина по 0,03—0,05 г 3 раза в день, длительностью 2—3 нед. Предполагают, что дифенин оказывает угнетающее действие на синаптическую проводимость и снижает посттетаническую активность в мышцах [Гехт Б. М., Ильина Н. А., 1982].
В настоящее время доступна пренатальная диагностика носительства гена миотонической дистрофии.
Прогрессирующая мышечная дистрофия
(миопатия Дюшенна) как самостоятельная клиническая форма в группе мышечных дистрофий достаточно хорошо изучена. Впервые она была подробно описана в 1868 г. Частота в популяции — 1:30 000.
Клиническая картина. Наблюдается почти исключительно у мальчиков. Основная симптоматика заболевания заключается в прогрессирующем нарастании дистрофических изменений с постепенным обездвиживанием больного.
Поражаются прежде всего нижние конечности. Первые симптомы появляются, как правило, в возрасте 2—4 лет, хотя до этого, уже на 1—2-м году жизни, двигательная активность больных обычно снижена. Дети позднее начинают ходить, не бегают, не влезают на стулья и т. п. В дальнейшем развивается специфическая («утиная») походка с переваливанием из стороны в сторону.
Характерны псевдогипертрофии икроножных мышц при нарастании диффузной мышечной атрофии. Икроножные мышцы становятся плотными, увеличиваются в объеме. Сухожильные рефлексы исчезают, но в ранней стадии заболевания они могут быть даже несколько повышены.
Процесс имеет восходящий характер: помимо ног, мышечная слабость распространяется на мышцы спины, грудной клетки, верхних конечностей. К 13—15 годам больные, как правило, полностью обездвижены. Смерть наступает в конце 2-го десятилетия чаще всего от острой сердечной недостаточности или от пневмонии.
По данным разных авторов, 30—70 % больных миопатией Дюшенна страдают умственной отсталостью. Последняя предшествует появлению мышечных нарушений и не нарастает, несмотря на прогрессирование самого заболевания .
Степень интеллектуального недоразвития может быть различной. Преобладают больные с негрубым снижением интеллекта, но встречаются случаи олигофрении в степени имбецильности.
Диагноз. Врожденный характер интеллектуального дефекта в сочетании с симптомами миопатии, проявляющимися на ранних стадиях главным образом запаздыванием в становлении моторики, нередко является причиной диагностических ошибок при обследовании ребенка в раннем возрасте В этих случаях иногда диагностируют остаточные явления органического поражения мозга с умственной отсталостью и атонической формой детского церебрального паралича.
При дифференциальном диагнозе должен учитываться характер мышечных нарушений: более резкое поражение проксимальных отделов мышц конечностей по сравнению с дистальными, очень резко выраженная гипотония мышц. В сомнительных случаях диагноз уточняют с помощью электромиографии. На ЭКГ — изменения, характерные для поражения мышц.
Прогрессирующая мышечная дистрофия Дюшенна вызывается рецессивным геном, локализованным в Х-хромосоме.
Патогенез умственной отсталости при этом заболевании до конца полностью неясен. Анатомических изменений в мозге, как правило, не обнаруживают, хотя описывают в отдельных случаях изменения корковой цитоархитектоники с гетеротопией нейронов.
Лечение. Эффективной патогенетической терапии нет. Проводят общеукрепляющее лечение, включающее биогенные стимуляторы, аутогемотерапию, витамины.
Используются в лечении больных препараты, улучшающие синтез белка, в частности анаболические гормоны (неробол, ретаболил). Наблюдался положительный эффект от применения аллопуринола — ингибитора ксантиноксидазы, участвующей в распаде пуринов, а также препаратов из группы -адреноблокаторов.
При решении вопроса о прогнозе потомства у женщин с установленным носительством гена миопатии Дюшенна методом выбора является определение пола плода.
Запись к врачу
Для того, чтобы записаться на цикл, выбирайте любой способ:
- звонок по телефону клиники +7 (495) 103-99-55,
- заказать обратный звонок,
- оставить заявку на запись на прием, через удобную форму на сайте:
ЗАПИСАТЬСЯ
В Кунцевском лечебно-реабилитационном центре, мы создали все условия, чтобы вы могли пройти реабилитацию с 8 утра до 10 вечера в будни и с 9 утра до 9 вечера в выходные.
Наш центр находится в шаговой доступности от метро «Молодежная».
Если вы на автомобиле, то приятным дополнением станет бесплатная парковка для наших посетителей.
РАБДОМИОЛИЗ
При травмах мускулатуры (чаще бывает у спортсменов) происходит постепенное разрушение тканей, это состояние называется рабдомиолиз. Этот процесс в итоге заканчивается отмиранием (некрозом) клеток и попаданием токсинов в кровеносную систему. Это заболевание может вызвать серьезные осложнения, привести к почечной недостаточности. При неоказании квалифицированной помощи может окончиться смертельным исходом.
Возможные причины:
1. Телесные повреждения (травмы, побои, аварии, несчастные случаи).
2. Ожоги 3-й и 4-й стадии.
3. Длительные хирургические операции (более 8–10 часов).
4. Длительные передавливания тканей с нарушением кровоснабжения.
5. Удары электротоком.
Спровоцировать развитие могут: повышенные нагрузки на тренировках, эпилептические припадки, сильные мышечные спазмы, белая горячка.
Распознать заболевание очень сложно, проявления схожи с симптомами многих заболеваний, иногда рабдомиолиз протекает скрытно. Часто поставить правильный диагноз можно только по результатам анализа крови. При запущенной форме пациент может впасть в кому и умереть.