Материалы и методы
В исследование было включено 109 больных РС (49 мужчин, 60 женщин; средний возраст – 33 года; диапазон – 17-54): 51 с вторично-прогрессирующим течением, 19 с первично-прогрессирующим, 8 с прогрессирующе-рецидивирующим и 31 с рецидивирующе-ремиттирующим течением. Значение индекса EDSS до трансплантации колебалось от 1.5 до 8.0 баллов (в среднем было равно 5.0 баллам). Длительность наблюдения составила в среднем 19 месяцев (от 6 до 108 месяцев). Активность заболевания определяли с помощью неврологического осмотра и данных магнитно-резонансной томографии. Больным были выполнены следующие виды ВДТ+АуТКСК: — Ранняя трансплантация
проводилась в дебюте заболевания при наличии неблагоприятных прогностических факторов в отношении химиорезистентности или возможности тяжелой инвалидизации больного.
— Этапная трансплантация
проводилась при выходе заболевания из-под контроля традиционных методов лечения и формировании вторичной химиорезистентности.
— Трансплантация спасения
проводилась в далеко зашедшей стадии заболевания при высокой активности иммунопатологического процесса и быстром прогрессировании инвалидизации больного. Тридцати двум больным была выполнена ранняя трансплантация (EDSS 1.5-3.0); 70 больным — этапная трансплантация (EDSS 3.5-6.5) и 7 больным — трансплантация спасения (EDSS 7.0-8.0).
Оценку клинического ответа и ответа, связанного с качеством жизни, проводили до трансплантации, при выписке из стационара, через 3, 6, 9 и 12 месяцев после трансплантации, затем – каждые 6 месяцев в течение первых 4 лет и ежегодно впоследствии. Изучение неврологического статуса включало определение выраженности неврологического дефицита по шкале EDSS и магнитно-резонансную томографию. Качество жизни больных 16 www.ctt-journal.com 2008;1(2) оценивали с использованием опросников FACT-BMT (функциональная оценка состояния больных после трансплантации костного мозга) и FAMS (функциональная оценка больных с рассеянным склерозом). Клиническим улучшением считали уменьшение выраженности неврологической симптоматики, по меньшей мере, на 0.5 балла по шкале EDSS по сравнению с исходным уровнем, при условии, что это улучшение было подтверждено через 6 месяцев на следующем визите. Любое увеличение выраженности неврологической симптоматики по шкале EDSS считали прогрессированием заболевания. Рецидив констатировали при появлении новых симптомов или нарастании выраженности прежних симптомов, по меньшей мере, в течение 24 часов в отсутствие лихорадки у пациента, который был стабилен в течение 4 предшествующих недель. Ответ, связанный с качеством жизни, характеризовался как минимальный, умеренный, хороший или максимальный. Для определения ответа, связанного с качеством жизни, рассчитывали различия в значении интегрального показателя качества жизни до проведения трансплантации и в различные периоды времени после нее.
Причины появления и развития рассеянного склероза
Основным источником развития патологии являются многочисленные вирусы — это краснуха, паротит, герпес, корь, бешенство и ряд других. Проникая в нервные клетки, они живут в них годами, разрушая как сами клетки, так и миелин. Болезнь развивается следующим образом.
- Разрушенные ткани постепенно заменяются прионом — чужеродным белком, играющим роль мощного антигена.
- На его появление и распространение иммунная система человека отвечает мощной аутоиммунной агрессией — происходит выработка антител.
- Последние направляются на уничтожение белого вещества нервных волокон, воспринимая его как чужеродный белок.
В результате иммунная система организма постепенно уничтожает нервную систему. В процессе развития патологии происходит поражение сразу нескольких ее отделов: оболочка постепенно разрушается и в ходе демиелинизации образуются очаги поражения — так называемые бляшки рассеянного склероза. Поскольку очаги поражения имеют рассеянный характер, склероз называется рассеянным. Само слово «склероз» в данном контексте означает «рубец» — это те самые спорадически распространяющиеся рубцы-бляшки (участки соединительной ткани), которые образуются на месте уничтоженных нервных тканей. Размер образований может доходить до нескольких сантиметров и более (если в ходе болезни они сливаются). Активные очаги, находящиеся в стадии образования, называют острыми.
Результаты
У всех 79 больных со сроком наблюдения ≥9 месяцев отмечено клиническое улучшение или стабилизация в течении заболевания. Во время проведения трансплантации не было зарегистрировано ни одного смертельного исхода и тяжелых неконтролируемых побочных эффектов. Через 6 месяцев после трансплантации распределение пациентов согласно клиническому ответу было следующим: улучшение – 42 (53%) больных, стабилизация – 37 (47%) больных. Среди больных с улучшением у 20 было вторично-прогрессирующее течение, у 7 – первично-прогрессирующее, у 4 – прогрессирующе-рецидивирующее и у 11 – рецидивирующе-ремиттирующее течение. В этой группе 25 больных проведена этапная трансплантация, 15 – ранняя и 2 – трансплантация спасения. Из 37 больных, у которых зарегистрирована стабилизация заболевания, у 19 было вторично-прогрессирующее течение, у 8 – первично-прогрессирующее, у 2 – прогрессирующе-рецидивирующее и у 8 – рецидивирующе-ремиттирующее течение. В этой группе 23 больным проведена этапная трансплантация, 9 – ранняя и 5 – трансплантация спасения.
В более длительные сроки наблюдения у 40 больных (50.6%) сохранялось улучшение, у 34 (43.1%) – стабилизация. У одного больного после 6 месяцев и двух больных после 18 месяцев стабилизации произошло повышение индекса инвалидизации. У двух пациентов прогрессирование заболевания наступило после 12 и 30 месяцев клинического улучшения. По данным МРТ у всех больных без прогрессирования заболевания после трансплантации отсутствовали активные или новые очаги поражения. В целом, 6-летняя выживаемость без прогрессии после ВДТ+АуТКСК составила 72%. Больные, у которых не было зарегистрировано признаков прогрессирования заболевания, не получали иммуномодулирующую или иммуносупрессивную терапию после трансплантации. Мониторинг качества жизни проводился у 44 пациентов, включенных в исследование. У 40 из них наблюдали улучшение показателей качества жизни через 6 месяцев после трансплантации. Улучшение параметров качества жизни установлено с помощью опросников – FACT-BMT и FAMS. Через 1 год после ВДТ+АуТКСК зарегистрировано следующее распределение пациентов в соответствии со степенью ответа, связанного с качеством жизни: у 3 больных наблюдали максимальный ответ (более чем 75% улучшение интегрального показателя качества жизни в сравнении с исходным уровнем); у 12 больных – хороший ответ (улучшение на 50-75%); у 11 больных – умеренный ответ (на 25-50%); у 13 – минимальный ответ (улучшение менее чем на 25%) и у 5 больных ответ, связанный с качеством жизни, отсутствовал. Следует отметить, что у пациентов с более длительным сроком наблюдения было отмечено дальнейшее улучшение показателей качества жизни. В статье представлена классификация типов трансплантации при рассеянном склерозе, основанная на концепции ВДТ+ТКСК при аутоиммунных заболеваниях.
Рассеянный склероз
Первое описание болезни было составлено неврологом Жаном Мартеном Ширко (Франция) в 1868 году. Рассеянный энцефаломиелит (а именно таково научное название этого недуга) — аутоиммунное прогрессирующее хроническое заболевание нервной системы, протекание которого сопровождается постепенным поражением миелиновой оболочки нервных волокон головного и спинного мозга. Волокна соединяют центры мозга посредством электрических импульсов, ускорение скорости которых и обеспечивает миелин — электролизующее белое вещество липидно-белкового происхождения. Помимо этой функции оболочка выполняет и другую, не менее важную, — миелин изолирует нервные отростки друг от друга.
Лечение РС стволовыми клетками в нашей клинике
Один из наиболее эффективных методов борьбы с коварным недугом — лечение рассеянного склероза стволовыми клетками. Именно этот прогрессивный и действенный метод заместительной терапии сегодня предлагается в передовых клиниках Санкт-Петербурга. Он обеспечивает:
- восстановление миелина, а вместе с ним — и нормальной скорости передачи нервных импульсов;
- регенерацию клеток головного и спинного мозга на участках нервных тканей, замещенных соединительной рубцовой тканью;
- нормализацию деятельности иммунной системы с прекращением аутоиммунных «атак» с ее стороны на нервную систему организма.
На раннем этапе развития болезни возможно излечение РС благодаря мощному регенеративному потенциалу стволовых клеток. Метод лечения рассеянного склероза стволовыми клетками характеризуется достижением высоких результатов: в каждом из имевших место случаев терапевтического воздействия он обеспечивает стойкую ремиссию. В результате проводимых терапевтических процедур пациенты клиники вновь обретают моторику двигательных функций, возможность полностью обслуживать себя, самостоятельно передвигаться, иными словами — возможность жить полноценной жизнью.
Описание и преимущества
В Arthrex Angel для приготовления концентрата используется собственный биологический материал пациента в закрытой стерильной одноразовой системе. Это полностью автоматизированная система, в которой используется технология 3-х сенсоров (3ST), она позволяет точно распределить компоненты крови или костного мозга на PRP / BMC (обогащенная тромбоцитами плазма), PPP (бедная плазма) и RBC (эритроцитов) в стерильные контейнеры. Технология 3ST является уникальной и позволяет достигать концентрацию в 18 раз выше от первоначальной.
Основной плюс системы в том, что пользователь может задавать желаемую концентрацию различных элементов в полученном полезном продукте (PRP, BMC или PRF/BMC gel), изменяя параметры центрифугирования. Это позволяет контролировать концентрацию тромбоцитов, лейкоцитов и эритроцитов, получая при этом желаемую пропорцию элементов в плазме. Это особенно важно, поскольку для каждого типа патологий наиболее эффективной является та или иная концентрация определенных элементов в конечном продукте.
Рассеянный склероз — клинические проявления
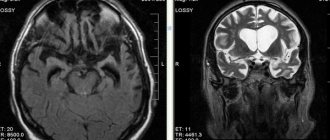
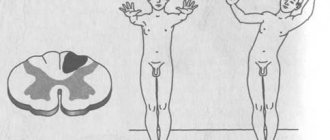
На фото: Бляшки — очаги демиелинизации
Клинические проявления РС — прямое следствие очаговых поражений отделов головного мозга.
Симптоматика рассеянного склероза сложна и разнообразна. В ряду наиболее частых характерных проявлений назовем следующие.
- Нарушения двигательной системы, связанные с поражением мозжечка, — у больного появляются пошатывания при ходьбе, возникает неловкость в движениях, нарушается координация, повышается мышечный тонус в руках. В отдельных случаях возникают парезы, случаются параличи.
- Нарушение зрения — возможно нарушение движения глазного яблока, появление «пелены» перед глазом или черной точки по центру поля зрения, при этом снижение зрения (вплоть до его потери) характерно для одного глаза.
- Нарушение функций тазовых органов — недержание мочи.
- Снижение вкусовой чувствительности.
- Поражение лицевого нерва с ослаблением мышц на одной стороне лица.
- Нарушения психической сферы — неврозоподобные состояния, астенический синдром, депрессия и т.д.
- Быстро наступающая усталость, утомляемость даже после незначительных физических и умственных нагрузок.
Рассеянный склероз
— весьма «коварное» заболевание: после появления первых проявлений симптоматика может исчезнуть на довольно длительный срок (даже на 10 — 15 лет), однако впоследствии, при отсутствии лечения болезни, она обязательно даст о себе знать в более тяжелых проявлениях. Кроме того, обострение болезни может быть спровоцировано перегреванием и переохлаждением, ОРВИ и другими заболеваниями, нервно-эмоциональными перегрузками.
Рассеянный склероз по степени тяжести
- Легкий тип: ремитирующее течение РС — обострения редки, периоды ремиссии — длительны.
- Среднее по тяжести течение — ремитирующе-прогрессирующее.
- Тяжелое, прогрессирующее течение (может быть первичным или вторичным).
Рассеянный склероз по форме
Форма рассеянного склероза определяется в зависимости от преобладающих симптомов. Выделяют спинальную, церебральную, глазную, гиперкинетическую, а также атипическую форму РС.
Группы и факторы риска
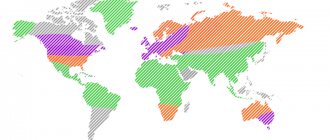
Темно-синим цветом выделены регионы с высоким риском заболевания РС, красным — с вероятно высоким риском.
Много ранее, задолго до появления технологии лечения рассеянного склероза стволовыми клетками, считалось, что основную группу риска составляют женщины в возрасте от 20 до 40 лет. Современный коллективный портрет больных весьма неоднороден: медики отмечают значительный рост случаев заболевания среди мужчин и женщин старше 40 лет. При этом у мужчин чаще всего протекает неблагоприятная прогрессирующая форма заболевания. Значительно чаще рассеянный склероз встречается сегодня среди европейцев — жителей северных регионов (Скандинавия, Северо-Запад России, Белоруссия). Таким образом, регион проживания сегодня признан одним из факторов риска, обусловливающих возможность появления рассеянного склероза. Помимо этого, в ряду других основных факторов:
- сосудистые заболевания;
- аутоиммунные заболевания;
- нарушенное психоэмоциональное состояние;
- инфекционно-аллергические заболевания;
- генетическая предрасположенность (изменение ферментных показателей, недостаточность Т-супрессоров).
Лечение рассеянного склероза
Этиотропная терапия РС, т.е. лечение, направленное на устранение конкретной причины заболевания, не практикуется в силу невозможности выявить его конкретный возбудитель. Вследствие этого применяется патогенетическая терапия, главными задачами которой являются:
- купирование обострения заболевания с воздействием на очаги аутоиммунного воспаления и одновременной активизацией компенсаторно-приспособительных механизмов;
- предотвращение и уменьшение выраженности обострений;
- симптоматическая терапия по устранению симптомов, негативно сказывающихся на возможности пациента вести привычный образ жизни.
В ходе лечения рассеянного склероза используются плазмаферез, глюкокортикоиды, копаксон, адренокортикотропный гормон, биостимуляторы, витамины группы В и другие препараты.